Белый фосфор, заключенный в нанотрубку, превратился в «розовый»

Исследователям из Великобритании удалось изолировать в одностенной углеродной нанотрубке цепочку из молекул белого фосфора, проявляющих высокую химическую активность. Прореагировав друг с другом, эти молекулы образовали полимерную структуру, получившую название «розовый фосфор». Новый аллотроп позволит ученым больше узнать о свойствах одного из самых реакционноспособных элементов Периодической системы, а также отследить первые этапы его превращения из активного белого фосфора в более инертную аллотропную модификацию — красный фосфор.
Аллотропия (от греческого allos — «другой» и tropos — «признак») — это существование двух и более простых веществ, образованных атомами одного и того же химического элемента и различных по строению и свойствам. Эти вещества называют аллотропными модификациями (или аллотропами) этого элемента. Аллотропия вызвана различным расположением атомов в кристаллической решетке (если речь идет о некоторых твердых аллотропных модификациях) или возможностью образования элементом нескольких видов молекул с различным составом (если говорить о веществах с молекулярным строением). Кристаллическое строение имеют аллотропы углерода алмаз, графит и графен (все они состоят из атомов углерода), молекулярное — аллотропы кислорода дикислород О2 и озон О3, аллотропы углерода фуллерены С60, С70, а также фосфор.
Классические аллотропные модификации фосфора известны давно. Это, во-первых, обладающий высокой реакционной способностью, светящийся в темноте и токсичный для человека белый фосфор. Он состоит из молекул Р4, в которых атомы фосфора расположены в вершинах тетраэдра. Во-вторых, это более устойчивый и менее ядовитый красный фосфор, применяющийся при производстве спичек. Это сложный полимер, в котором нити из атомов фосфора сшиты друг с другом; его молекулы гораздо больше, чем у белого фосфора. Еще один аллотроп фосфора — исключительно инертный черный фосфор, строение кристаллической решетки которого подобно строению графита.
Всё это время химики знали, какие условия нужно создать для превращения одной модификации в другую, но практически не представляли себе, что же конкретно происходит с атомами фософра при превращении белого фосфора в красный (этот процесс не изучали ни экспериментально, ни с помощью квантовохимических симуляций), а красного — в черный. Интерес к химии аллотропных модификаций фосфора возобновился лишь через сто лет после обнаружения черного фосфора, в 2014 году, когда был открыт очередной аллотроп этого элемента — фосфорен (см. Han Liu et al., 2014. Phosphorene: An Unexplored 2D Semiconductor with a High Hole Mobility), фосфорный аналог графена.
Одна из причин такого пробела в наших знаниях об аллотропных переходах фосфора заключается в том, что белый фосфор представляет собой чрезвычайно опасное и химически активное вещество, которое может самовозгораться от контакта с воздухом. Продукт его горения, оксид фосфора P4O10, вступает в реакцию с парами воды, давая в итоге обладающую высокой коррозионной способностью фосфорную кислоту H3PO4. А что касается компьютерного моделирования процессов полимеризации, в которых участвует большое количество частиц, то оно требует привлечения значительных вычислительных мощностей, которые далеко не всегда доступны.
Ранее предпринимавшиеся попытки «укротить нрав» белого фосфора позволили разработать супрамолекулярные «клетки» (см. Супрамолекулярная химия), которые могли вместить только одну молекулу P4 (см. Prasenjit Mal et al, 2009. White Phosphorus Is Air-Stable Within a Self-Assembled Tetrahedral Capsule). Такие молекулярные контейнеры, с одной стороны, позволяли избежать реакции белого фосфора с водяными парами воздуха, но с другой — не могли служить системами для изучения аллотропного перехода из белого фосфора в красный. Дело в том, что красный фосфор представляет собой полимерную структуру, и для превращения белого фосфора в красный необходима реакция присоединения молекул Р4 друг к другу, а супрамолекулярный резервуар изолирует их и тем самым делает такую реакцию невозможной.
В группе профессора Университетского колледжа Лондона Кристофа Зальцманна (Christoph G. Salzmann) решили использовать другой вариант «клеток» для белого фосфора. Эти исследователи попробовали изолировать его молекулы от кислорода и влаги воздуха, но при этом дать им возможность сближаться друг с другом. Для решения такой задачи в качестве контейнеров для упаковки молекул Р4 были выбраны одностенные углеродные нанотрубки (ОУНТ) с внутренним диаметром 8,1 Å. ОУНТ — еще одна аллотропная модификация углерода, которую можно представить как листок графена, свернутый в трубочку. Хотя внутренний диаметр выбранных для эксперимента нанотрубок вполне подходил по размерам для получения соединений включения P4@ОУНТ, самой сложной задачей было заполнение нанотрубок белым фосфором. Тут пришлось на длительное время «замачивать» углеродные нанотрубки в расплавленном белом фосфоре, а для выполнения такой работы воистину нужны золотые руки и стальные нервы, ведь, как уже говорилось выше, этот аллотроп фосфора легко самовоспламеняется.
Для работы были взяты одностенные углеродные трубки, закрытые с одной стороны полусферической головкой, которая ограничивала доступ кислорода, воды и других веществ к молекулам Р4. С другой стороны нанотрубки были открыты. Через открытый конец («горлышко») в них попадали молекулы Р4, а после заполнения трубок их подвергали воздействию воздуха, который окислял молекулы в непосредственной близости к «горлышку». Продукты окисления при этом играли роль пробки, изолировавшей белый фосфор внутри нанотрубки.
Для доказательства того, что нанотрубки заполнены, полученные соединения включения (такие соединения образуются путем включения молекул-«гостей» в полость одной большой молекулы-«хозяина»; см. также Связанные водородной связью молекулы поймали в клетку фуллерена, «Элементы», 30.05.2017) изучали целым набором физических методов, включая просвечивающую электронную микроскопию высокого разрешения (ПЭМВР; см. Просвечивающий электронный микроскоп). Результаты исследования показали, что молекулы P4 заполняют углеродные нанотрубки подобно тому, как горошины располагаются в стручке (рис. 2).
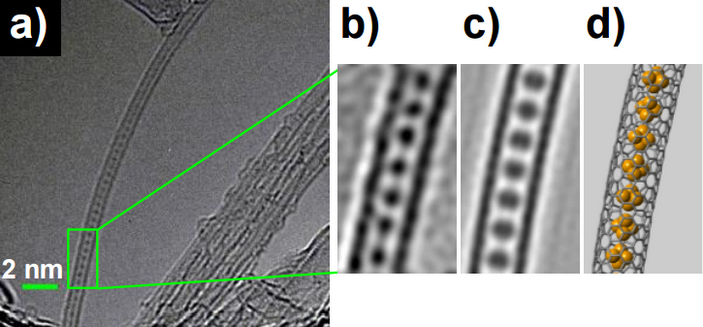
Рис. 2. Как горошины в стручке: одностенная углеродная нанотрубка (ОУНТ), заполненная молекулами белого фосфора P4; a) — полученное с помощью просвечивающей электронной микроскопии высокого разрешения (ПЭМВР) изображение одностенной углеродной нанотрубки с цепочкой молекул P4 внутри. b) — изображение выделенного на (а) участка после подавления шумов; c) — симуляция изображения ПЭМВР; d) — схематичное строение соединения включения P4@ОУНТ. Масштаб изображений b)–d) одинаков. Рисунок из обсуждаемой статьи в Angewandte Chemie International Edition
Электронный микроскоп не только позволил подтвердить строение соединений включения: к удивлению исследователей было обнаружено, что пучок электронов, необходимый для получения изображения в методе ПЭМВР, инициировал сшивание молекул P4 в цепную структуру — новую аллотропную форму фосфора, «розовый фосфор» (рис. 3). Такое название новой форме фосфора было дано из предположения, что образование линейной полимерной цепи из атомов фосфора представляет собой первую стадию перехода белого фосфора в красный. Возможно, вне углеродной нанотрубки цепи розового фосфора начинают взаимодействовать друг с другом, образуя сшитый полимер, известный нам как красный фосфор.

Рис. 3. Полимеризация молекул P4 внутри одностенной углеродной нанотрубки. a) и b) — полученное с помощью ПЭМВР изображение одностенной углеродной нанотрубки с продуктами полимеризации фосфора; c) — изображение выделенного на (b) участка после подавления шумов; d) — симуляция изображения ПЭМВР; e) — схематичное строение соединения включения зигзагообразная цепь P4@ОУНТ. Масштаб изображений c)–e) одинаков. Рисунок из обсуждаемой статьи в Angewandte Chemie International Edition
Полученная в нанотрубке нить «розового фосфора» интересна не только как интермедиат в аллотропных переходах. Предварительные расчеты показали: не исключено, что такой аллотроп фосфора обладает интересными электронными свойствами. Однако, чтобы это выяснить, необходимо разработать способ оценки электронных свойств цепочки розового фосфора, который позволил бы исключить влияние углеродной нанотрубки на результаты измерений: дело в том, что ОУНТ являются хорошими проводниками.
Если изменить диаметр нанотрубок и научиться помещать в них сразу нескольких «ниток» из Р4, то химики рано или поздно получат возможность наблюдать не только за образованием одной нити из атомов фосфора, но и за сшивкой таких нитей — вероятно, именно она служит следующим шагом перехода «белый фосфор — красный фосфор». Исследователи уже провели компьютерное моделирование реакций, которые могут протекать с участием молекул Р4 и продуктов их превращений в нанотрубках большего диаметра, и сделали ряд предположений о том, какие структуры будут с наибольшей вероятностью получаться в таких нанореакторах из атомов углерода.
Источник: Martin Hart et al. Encapsulation and Polymerization of White Phosphorus Inside Single-wall Carbon Nanotubes // Angewandte Chemie International Edition. 2017. Accepted Author Manuscript. DOI: 10.1002/anie.201703585.
См. также:
Связанные водородной связью молекулы поймали в клетку фуллерена, «Элементы», 30.05.2017.
Аркадий Курамшин
И - по поводу причин неизученности ряда модификаций фосфора. Конечно, причина вовсе не в ядовитости или же пожароопасности. И красный, и белый фосфор - крупнотоннажные продукты, работать с такими веществами давно умеют. Достаточно вспомнить классические работы Н. Семенова по кинетике окисления, легшие в основу теории цепных реакций. Да и нужно в лаборатории не тонны, а самое большее граммы вещества. С зарином- зоманом работают, с металлорганикой вроде диалкилцинка, которая воспламеняется мгновенно на воздухе - тоже, а тут, значит, страшно боятся. Вопрос не в опасности, а в том, что то ли руки не дошли, то ли не было ясности, какую-такую полезную информацию можно почерпнуть.
-
Насчет ошибки с "соединением" - согласен - досадная опечатка вышла, надо было просто "вещество" написать, тут не поспоришь. У самого автора в моем лице допуска к правкам уже выгруженного материала нет, надеюсь, редакция поправит.
Насчет второго - вопрос дискуссионный на самом деле. Крупнотоннажность продукта и его производство в промышленности не означает, что лаборатории с ним работать не страшно - все же в промышленном цехе, производящем, скажем, белый фосфор и в лаборатории разные параметры работы приточной вентиляции, разная оснащенность СИЗ и т.д. Скажем так, видел я цеха в которых с окисью этилена работают, так там по ТБ окна полиэтиленом занянуты, а не остеклены - на случай взрыва, чтобы осколками не побило.
Опять же, одно дело литий- или цинкорганика, которая в стекле работает в синтезе, но для изучения механизма реакции даже простой ИК-спектрометр уже проблемно вводить в контакт с парами белого фосфора и продуктами его реакций с компонентами атмосферы - закоротят пары фосфорной кислоты схемы и всё... Я не говорю про более дорогостоющую технику
Понятно, что тот же белый фосфор можно плавить в glovebox под аргоном, как и работают с металлоорганикой, что, собственно авторы и делали, чтобы им зарядить нанотрубки, и все было нормально, но, поскольку на эксперимент еще и средства нужно получить в виде внутреннего или внешнего гранта, и коллег по этажу предупредить, думаю - в данном случае риск от того, что что-то пойдет не так, выше возможной выгоды.-
И все же: опасность белого фосфора не нужно преувеличивать. Во времена не столь уж давние (вплоть до начала 20 века) именно белый фосфор использовали при изготовлении спичек. Ну да ладно.
Смущает вот что: можно ли то, что получили британцы, считать новой аллотропной формой фосфора? А может, мы имеем дело с вульгарной капиллярной конденсацией? Способна ли эта нить существовать, хоть и кратковременно, вне трубок? И не получается ли так, что теперь и любые клатраты, любые адсорбированные состояния (скажем, воду в составе цеолитов или же метан в составе гидратов) нужно считать новой полиморфной модификацией?
Смущает и вот еще что. Не слишком ли много внимания "британским ученым"? Вспомните: нобелевки выданы и за фулерены, и за изучение графена - а кто-то хотя бы помнит о том, что в СССР была открыта интереснейшая кумуленовая форма углерода с линейными молекулами? Алексей Михайлович Сладков не только выделил это вещество - он разработал несколько методов синтеза, изучил основные свойства, доказал линейность строения. И остался в забвении.
"Элементы" - наверное, единственный у нас популярный сайт о науке, который не впадает в крайний примитивизм, не гонится за дешевкой и дает информацию, предоставляемую если и не специалистами, то, по крайней мере, людьми " в теме" - а потому было бы очень здорово, если бы тут появилась статья о карбине и А.М. Сладкове. Это был невероятно интересный человек.
-
Интересно, если не использовать электронный пучок будет ли протекать полимеризация или мы увидим лишь разрозненные группы молекул тетрафосфора?
Последние новости













Рис. 1. Химики из Великобритании заполнили одиночными молекулами белого фосфора углеродные нанотрубки (слева) и выявили условия, в которых эти молекулы превращаются в полимерную нить «розового фосфора» — промежуточное соединение между ядовитым белым и менее опасным красным фосфором, используемым в том числе в производстве спичек. Рисунок из обсуждаемой статьи в Angewandte Chemie International Edition