Процесс появления новых ферментов прослежен в эволюционном эксперименте

Эксперименты на бактерии Salmonella enterica показали, что новые ферменты могут возникать по схеме «инновация — амплификация — дивергенция». Сначала у фермента в результате мутации появляется дополнительная каталитическая активность («инновация»). Если новая функция окажется полезной, отбор поддержит амплификацию (появление дополнительных копий) измененного гена. В дальнейшем с большой вероятностью произойдет разделение труда между копиями («дивергенция»): одни копии оптимизируются отбором для выполнения старой функции, другие — для новой. В строгом соответствии с этой схемой из фермента, участвующего в синтезе аминокислоты гистидина, в ходе эволюционного эксперимента был получен фермент, катализирующий один из этапов синтеза триптофана.
Теоретические сценарии
Новые гены, как правило, появляются из старых в результате амплификации (увеличения числа копий гена, см. Gene duplication) с последующим разделением функций между копиями. Новая функция может появиться у одной из копий уже после амплификации. Альтернативный вариант — появление дополнительной функции у гена еще до того, как он подвергся амплификации (подробнее см. в заметке Многофункциональные гены — основа для эволюционных новшеств, «Элементы», 30.06.2008).
В обоих случаях обязательным этапом является закрепление полезных мутаций в одной или нескольких копиях гена после амплификации. Проблема в том, что эти полезные мутации должны закрепиться быстро — до того, как «избыточные» копии гена будут испорчены вредными мутациями или вовсе потеряны. Если отбор не воспрепятствует повреждению этих копий, то они, скорее всего, будут безнадежно испорчены раньше, чем в них возникнет какая-то полезная мутация (потому что вредные мутации возникают намного чаще, чем полезные). В итоге всё вернется на круги своя, и в геноме снова останется только одна рабочая копия гена плюс некоторое количество «мусора» — испорченных мутациями псевдогенов, в которые превратятся остальные копии.
Биологи из Швеции и США предложили и экспериментально проверили сценарий появления новых генов, который они назвали IAD (innovation-amplification-divergence, инновация — амплификация — дивергенция). Сценарий похож на известный механизм «ухода от адаптивного конфликта», о котором рассказано в вышеупомянутой заметке, но имеет одно существенное отличие. В сценарии IAD амплификация сама по себе имеет адаптивный смысл, то есть новообразованные копии гена с самого начала не являются «избыточными»: они полезны, и поэтому отбор препятствует их порче. Это дает им время дождаться появления полезных мутаций.

Рис. 2. Образование нового гена по схеме «инновация — амплификация — дивергенция». Пояснения в тексте. Изображение из обсуждаемой статьи в Science
Схема IAD показана на рис. 2. У гена с основной функцией А появляется (или существует изначально в качестве «побочного эффекта») дополнительная функция B, которая поначалу осуществляется с низкой эффективностью (и потому обозначается как b). Если эта побочная функция вдруг окажется полезной (например, из-за изменения условий среды), то отбор начнет поддерживать мутации, усиливающие эту функцию. Простейшим способом добиться этой цели, не нарушив функцию А, является амплификация бифункционального гена. Чем больше копий гена будет в геноме, тем больше будет молекул соответствующего белка и тем эффективнее будет осуществляться функция B. Таким образом, отбор будет поддерживать дупликации гена и защищать появляющиеся дополнительные копии от мутационных повреждений. Авторы отмечают, что амплификация генов — весьма распространенная категория мутаций. Например, у бактерии Salmonella enterica, с которой они работали, вероятность дупликации любого гена составляет примерно 10–5 на каждое клеточное деление.
После этого размножившиеся копии гена смогут специализироваться. Если в одной из копий возникнут мутации, усиливающие функцию B в ущерб A, то отбор их поддержит, ведь функция B «в дефиците», а с функцией A успешно справляются другие копии. У какой-то из них функция А может дополнительно оптимизироваться — возможно, за счет полной утраты функции B.
После появления генов-«специалистов», оптимизированных для эффективного выполнения функций A и B, остальные копии станут действительно лишними. Тогда они, скорее всего, быстро псевдогенизируются или будут утрачены.
Экспериментальное подтверждение
Для проверки своих идей авторы поставили эволюционный эксперимент на сальмонеллах. Для начала они взяли бактерий, из генома которых был удален ген trpF. Фермент, кодируемый этим геном, катализирует один из этапов синтеза аминокислоты триптофана. Похожий этап в синтезе другой аминокислоты, гистидина, катализируется ферментом hisA. Выращивая сальмонелл, лишенных гена trpF, в среде, не содержащей триптофана, исследователи обнаружили бактерий, у которых произошла спонтанная мутация (точнее, комплекс из двух мутаций — удвоение трех кодонов и замена одной аминокислоты) в гене hisA. В результате фермент hisA стал бифункциональным. Он приобрел способность выполнять функцию trpF, хоть и с низкой эффективностью. Исходная функция hisA при этом пострадала, то есть синтез гистидина стал менее эффективным. Но всё же бактерии-мутанты приобрели способность к медленному росту в среде, не содержащей ни триптофана, ни гистидина. Таким образом, возникшую мутацию можно рассматривать как первый этап — «инновацию» в сценарии IAD. Теперь нужно было проверить, осуществимы ли остальные два этапа.
Бактерий-мутантов разделили на несколько линий, которые выращивались изолированно друг от друга в среде без триптофана и гистидина. Чтобы отслеживать генные дупликации, рядом с hisA исследователи поместили ген желтого флюоресцирующего белка yfp, так что о количестве копий данного фрагмента генома можно было судить по силе флюоресценции. Поскольку мутантный фермент hisA обе свои функции выполнял плохо, поначалу бактерии росли медленно, удваивая свою численность за 5,1 часов. Для сравнения, в среде с триптофаном у этих бактерий от одного деления до другого проходило 2,8 часов, с гистидином — 2,6, с обеими аминокислотами — 1,5.
Однако уже через несколько сотен поколений скорость размножения бактерий во многих линиях существенно увеличилась. Это произошло, как и предполагалось, за счет амплификации бифункционального гена. В некоторых линиях появилось до 20 копий hisA. В результате количество производимого клетками фермента увеличилось, и обе аминокислоты стали синтезироваться быстрее. Таким образом, второй этап предполагаемого сценария — амплификация — тоже подтвердился.
Эксперимент продолжался 3000 поколений, и за это время мутации, ускоряющие рост, закрепились во всех линиях. При этом в большинстве линий появились ферменты-«специалисты», эффективно выполняющие одну из двух функций. В некоторых случаях это сопровождалось потерей лишних копий (две копии становились «специалистами», остальные терялись). Эти результаты соответствуют предсказаниям модели IAD. Но было обнаружено и кое-что неожиданное: в некоторых линиях под действием мутаций и отбора сформировался фермент-«генералист», хорошо справляющийся с обеими функциями одновременно.

Рис. 3. Четыре примера эволюционных траекторий, зафиксированных в эксперименте. Ромбики соответствуют разным версиям фермента hisA. На графиках по горизонтальной оси отложена эффективность синтеза гистидина (она оценивалась как скорость роста бактерий в среде с триптофаном без гистидина), по вертикальной — эффективность синтеза триптофана (измеряемая как скорость роста в среде с гистидином без триптофана). Все подопытные линии изначально имели одну копию гена с мутациями dup13-15 и D10G. Такой фермент выполняет обе функции, но с низкой эффективностью. В случае А после амплификации одна из копий исходного гена оптимизировалась для синтеза гистидина, утратив способность синтезировать триптофан (D10G), другая оптимизировалась для синтеза триптофана и разучилась синтезировать гистидин (dup13-15, D10G, G81D). В случаях B и C исходный ген сначала приобрел мутацию G102A, что сделало его более эффективным «генералистом», но затем он амплифицировался, и разные его копии специализировались для выполнения двух функций по отдельности. В случае D сформировался высокоэффективный фермент-генералист с мутациями dup13-15, D10G, G102A, G11D, G44E. Синими ромбиками показаны генетические варианты, которые на каких-то этапах эволюции были единственными в своей популяции, желтыми — те, вместе с которыми всегда присутствовали другие варианты гена hisA. Изображение из обсуждаемой статьи в Science
Таким образом, эксперимент наглядно показал, что сценарий «инновация — амплификация — дивергенция» вполне реалистичен. Не исключено, что многие новые гены в ходе эволюции возникли именно таким путем. Но, пожалуй, больше всего поражает в этой статье ее спокойный тон и немного скучноватый стиль, как будто подчеркивающий, что воспроизводить в пробирке фундаментальные эволюционные события уже становится рутинным занятием для биологов.
Источник: Joakim Näsvall, Lei Sun, John R. Roth, Dan I. Andersson. Real-Time Evolution of New Genes by Innovation, Amplification, and Divergence // Science. 2012. V. 338. P. 384–387.
См. также:
Многофункциональные гены — основа для эволюционных новшеств, «Элементы», 30.06.2008.
-
Ожидаемая статья. У креационистов опять "пичалька". Помнится год назад Имперор с пеной у рта мне тут доказывал, что ни одного факта появления новых ферментов не зарегестрировано, поэтому эволюции нет. Как всегда наука и время работают против креационистов.
-
Нет, что Вы.
Вряд ли здесь можно говорить о "новом" ферменте в полном смысле этого слова. Дело в том, что авторы статьи взяли для работы именно такой фермент, который уже исходно обладал способностью к БИфункциональной работе.
К сожалению, у меня нет доступа к оригинальной статье. Но в любом случае, фермент, с которым работали авторы, либо был УЖЕ бифункциональным, либо спокойно мог им стать. Поскольку фермент относится к группе именно таких изоферментов, часть которых уже обладает той самой двойной активностью, о которой идет речь в статье.
Вот ссылка:
http://www.jcvi.org/cgi-bin/tigrfams/HmmReportPage.cgi?acc=TIGR01919
Как видите, фермент из этой группы УЖЕ работает и с гистидином и с триптофаном БЕЗ каких-либо «мутаций и эволюций».
Авторы оригинальной статьи, конечно, знали, с какими «новыми» ферментами они работают. И именно поэтому:
"...в этой статье спокойный тон и немного скучноватый стиль..."
Т.е. это Вы просто купились (в очередной раз) на слишком громкий и восторженный тон нашего "народного просветителя" (А. Маркова), где весьма скромные результаты преподносятся в качестве... (как он там написал?)... "фундаментальных эволюционных событий".
Т.е. мы в очередной раз наблюдаем, как «доказательства эволюции» выводятся (А. Марковым) не столько из фактического материала, сколько создаются путем употребления соответствующих (победных) оборотов речи и интонаций.-
И по философии у вас двоечка. Что подразумевали, когда говорили, что фермент мог "спокойно ... им стать". Значит, измениться? Значит, мутировать? Одна мутация для вас не эволюция, а много? Один год для эволюции, как может показаться, мало, а миллиард - это как, много?
Человек интуитивно меряет время относительно своей жизни, а 10 миллионов своих жизней по длительности представить дано не каждому, если такие посты появляются вновь.-
"...Что подразумевали, когда говорили, что фермент мог..."
Выше я уже привел ссылку для пояснения того, что я подразумеваю. На мой взгляд, эта ссылка исчерпывающе поясняет ситуацию.
P.s. К сожалению, сайт elementy.ru активно использует административный ресурс для подавления любых точек зрения (на "теорию эволюции"), которые сколько-нибудь заметно отличаются от того, что считает по этому поводу Александр Марков. В частности, новоиспеченный ник Imperorr_8 уже успели забанить (всего после одного комментария строго по теме заметки). Поэтому дальше беседуйте на эту тему сами с собой.-
Говорите покороче и пояснее -- и Вас не будут банить. Лично я, например, Вашу точку зрения не понял. Вы считаете, что изменение генов, заявленное в статье, не происходило?
-
Уважаемые dims и olegov! Имперор (во всех его прошлых и будущих ипостасях) на сайте "Элементы" забанен, и не надо, пожалуйста, его провоцировать на очередную дискуссию.
-
Уважаемый editor.
А теперь то за что? Вроде бы, все мои комментарии были строго по теме заметки?
P.s. И кстати. Советую обратить Ваше (такое беспристрастное) внимание вот на эту тему и комментарии к ней:
http://elementy.ru/news?discuss=431855
Вероятно теперь, после того, как Ваше внимание привлечено к этим комментариям, на сайте элементы.ру следует ожидать массовых банов? :)-
> А теперь то за что?
Просто забаненный однажды забанен навсегда. Ведь от того, что вы регистрируетесь под другим ником, вы не становитесь другим человеком.
Поскольку к вам обратились, мы дали вам возможность ответить, но дискуссий больше не будет.
> Советую обратить Ваше (такое беспристрастное) внимание вот на эту тему и комментарии к ней.
Спасибо. Забанить, наверное, не забаним, но офтопик сотрем.-
...Просто забаненный однажды забанен навсегда. Ведь от того, что вы регистрируетесь под другим ником, вы не становитесь другим человеком...
Всё-таки остаётся не совсем понятным, что со мной, собственно, не так (как с человеком).
Впрочем, не буду придираться. Я тоже думаю, что в случае возникновения серьезного конфликта одного из читателей сайта с одним из работающих авторов заметок, администрация, конечно, вынуждена выбирать в пользу работающего автора.
P.s. Спасибо, что на этот раз дали спокойно ответить на посты оппонентов.
-
-
-
-
-
-
Батенько, фермент ПРЕОБРАЗОВАЛСЯ. И это факт. Мало того, произошло формирование эволюционного новшества, не просчитанного заранее: сформировался еще и принципиально новый фермент, способный эффективно синтезировать обе аминокислоты. Так что эволюция - очевидная, фактическая эволюция - идет и здесь. А Вы - про "низенько-низенько":))))
-
-
-
-
Так в чём жульничество авторов статьи? Они же зафиксировали изменение гена. В чём враньё? На самом деле ген не изменялся?
-
Выше я уже высказался, как мне кажется, весьма коротко и достаточно ясно.
Хорошо, попробую еще раз более подробно:
1. Чисто ФОРМАЛЬНО, если мы НЕ будем углубляться ни в какие подробности, то действительно получается, что "родился" новый ген (т.е. казалось бы, вот оно - "фундаментальное эволюционное событие").
2. Но если мы попробуем разобраться, что же там произошло НА САМОМ ДЕЛЕ, то узнаём, что в природе у разных организмов имеются (по факту) ферменты (именно этой группы), УЖЕ работающие и с гистидином и с триптофаном, как по отдельности, так и одновременно. Этого обстоятельства уже достаточно, чтобы навести на соответствующие сомнения - так ли уж ново эволюционное приобретение.
Действительно (скорее всего) работа ферментов этой группы заключается в изомеризации аминоальдозы, которая является ОБЩИМ компонентом и гистидина, и триптофана. Т.е. по сути, фермент (после некоторых модификаций) продолжает выполнять всё ТУ ЖЕ биохимическую работу (только в разных веществах).
3. Когда речь идет о примерах появления новых ферментов, мы всё-таки представляем себе именно новые ферменты, демонстрирующие химическую активность к какому-то совершенно новому (для них) субстрату. Понятно, что данное исследование к такому случаю не относится.
Тем не менее, исследование еще раз подтвердило (вместе с другими более ранними аналогичными исследованиями), что в некоторой степени ферменты могут варьировать. Однако вопрос – насколько серьезными могут быть эти вариации, способны ли они порождать (теоретически постулируемые) принципиально новые типы химической активности – этот вопрос по-прежнему остаётся открытым.
4. Суть моего комментария (адресованного гражданину olegov) заключалась в следующем - Александр Марков предпочел пересказать результаты данного исследования в (победном) стиле наблюдаемого «фундаментального эволюционного события» (на что и купился гражданин olegov). А я говорю, что на самом деле, продемонстрированные факты весьма неоднозначны - они могут быть интерпретированы по-разному, в том числе, и весьма скромно. Поэтому «рапортовать» здесь следовало бы гораздо осторожней.-
Сударь, по поводу п.2 Вам как рази показано не только, КАК может родиться новый ген (в исходной популяции он ОТСУТСТВУЕТ и триптофан формируется иным геном, причем с хреновым выходом), но и как может родиться ИМЕННО ТАКОЙ ген, какой мы знаем - здесь двойной успех. Насчет п.3 - действительно, тема для других работ, и это ничем не умаляет достоинства этой. Но для иных типов химической активности нужно,чтобы оные были полезны для клетки, огромная вероятность, что ближний круг доступных химических соединений, потенциально полезных для жизни, уже давно "выбран" в процессе эволюции. Так что искать, собственно, уже нечего - все найдено естественным отбором и наследственной изменчивостью (с учетом частоты возможных мутаций по штуке в среднем на каждый ген за миллиард циклов репродукции и того, что этот генетический котел "варится" непрерывно уже миллиарды лет). А что касаемо п.4 - см. комментарии по п.2. Все предельно однозначно. Это факты. Против которых не попрешь))
-
> на соответствующие сомнения - так ли уж ново эволюционное приобретение
Авторы и не утверждали глобальную новизну фермента. Они проследили его образование и новизну для данного конкретного экспериментального организма.
> речь идет о примерах появления новых ферментов, мы всё-таки представляем себе именно новые ферменты
Понятно: Вам нужны ферменты, настолько новые, что у них даже нет аналогов на Земле. Окей, Ваша точка зрения понятна, но претензий к авторам статьи Вы обосновать не можете: они такого критерия к своим результатам не заявляли.
> способны ли они порождать (теоретически постулируемые) принципиально новые типы химической активности – этот вопрос по-прежнему остаётся открытым
Для Вас -- может быть. Для меня -- нет. И вообще это требование выглядит ненормальным.
> в (победном) стиле наблюдаемого «фундаментального эволюционного события»
Глупости. Никто не воюет с креационистами и, следовательно, никто не объявляет над ними никаких побед. Их просто не считают за противников. Эксперимент был поставлен в интересах самой науки, для удовлетворения ЕЁ потребностей в "фундаментальном эволюционном событии". Поэтому, раз заказчик считает, что заказ выполнен -- значит он выполнен. Мнение посторонних свидетелей о качестве выполнения заказа не имеет значения.-
1. К самим авторам оригинального исследования никто особенных претензий здесь не имел. Я высказался исключительно по заметке Александра Маркова (а не оригинальной статьи).
2. Каких еще "ферментов, которых нет на Земле"? Вы либо неправильно меня поняли, либо сознательно искажаете мою мысль.
Я имел в виду (в качестве возможного примера), что был некий исходный фермент, и он мутировал ТАК, что у него появилась какая-то пусть и минимальная, но химическая активность по отношению к НОВОМУ для НЕГО (а не вообще для Земли :) типу субстрата. И далее это свойство бы постепенно амплифицировалось.
Вот это и был бы хороший пример появления нового фермента real-time.
Причем заметьте, я вовсе НЕ отрицаю такую (принципиальную) возможность (я не знаю, кто здесь мне это приписал - видимо, на меня здесь решили навесить сразу всех "креационистcких собак" :) Я говорю лишь о том, что пока таких фактов не установлено, а успех озвученного здесь исследования, к сожалению, "смазывается" хорошо известной потенциальной бифункциональностью исходного фермента (именно по озвученным субстратам).
3. По поводу "войн с креационистами". Уважаемый dims. Понимаете, это просто поразительно - такое ощущение, что Вы вообще ничего не слышали о "тысяче и одной" дырках (т.е. о крайне слабых местах) современного эволюционного учения. Я не знаю, как это Вы смогли избежать знакомства со всеми (столь многочисленными) трудностями эволюционного учения (которые совершенно серьезно обсуждались и продолжают обсуждаться в научной литературе).
-
-
-
Креационисты не понимают, что если бы мы действительно в эксперименте вывели из собаки жука или кошку, то тем самым не подтвердили бы, а опровергли современную эволюционную теорию. Эволюция основана на медленном накоплении множества мелких изменений. Путь от собаки до жука у природы занял примерно 600+600=1200 миллионов лет. Это по минимуму, скорее ближе к 1,5 миллиарда (от собаки назад до общего предка, который жил в глубоком докембрии, а потом от него - вперед к жуку). Если бы такое воспроизводилось в лаборатории... вот тогда смело можно было бы заявить, что "Дарвин был неправ".
Имперор пишет "подумаешь, изменился фермент, который МОГ измениться, был к этому как бы готов".
Креационисты путают науку с (более привычными им?) религиозными чудесами. Они хотят чуда. Они требуют: сделайте нам такое эволюционное изменение, которое НЕ может произойти, тогда мы признаем эволюцию!
Разумеется, в эксперименте длиной в 3000 поколений были продемонстрированы как раз такие эволюционные изменения, которые МОГУТ произойти за 3000 поколений. А те, которые не могут произойти за такой срок (или не могут вовсе - эволюция ведь, в отличие от Ктулху, далеко не всесильна), конечно, не были в этом эксперименте продемонстрированы.
А у этого фермента, о котором речь, изначально НЕ БЫЛО второй активности. У данного вида бактерий в геноме два разных гена - один для синтеза триптофана, другой для гистидина. Это исследование началось с того, что бактерий с отключенным триптофановым геном выращивали на среде без триптофана.При этом авторы нашли мутанта, у которого гистидиновый фермент в результате мутации смог с трудом, но все же выполнять "триптофановую" функцию наряду с исходной (которая, впрочем, пострадала). В общем, см. заметку. В итоге из фермента только с одной (гистидиновой) функцией в эксперименте был выведен сначала малоэффективный фермент с двойной функцией, затем эффективный фермент с триптофановой функцией, эффективный фермент с гистидиновой функцией (эта функция восстановилась) и фермент, эффективно справляющийся с обеими функциями.
Да, у некоторых других микробов есть подобный фермент с двойной функцией. Но не у сальмонеллы энтерика, о которой речь в статье. У нее нет такого фермента. А то, что такие ферменты существуют у других микробов, действительно доказывает, что подобное эволюционное превращение возможно. Разумеется, оно возможно. Невозможные вещи пусть Имперор в молитвах у своих богов требует. А в научном эксперименте, как ни удивительно, можно продемонстрировать только возможные вещи.
-
По идее вроде бы это правдоподобно (хотя не из-за тРНК, они в другом месте, а из-за частой транскрипции). Но отбор перекрывает этот эффект, если он есть, так что на практике видим скорее обратное: "нагруженные работой" гены меняются медленнее, т.к. изменения в них эффективно отсеиваются отбором. Причем это касается, по-видимому, даже синонимичных замен
"Я имел в виду (в качестве возможного примера), что был некий исходный фермент, и он мутировал ТАК, что у него появилась какая-то пусть и минимальная, но химическая активность по отношению к НОВОМУ для НЕГО (а не вообще для Земли :) типу субстрата. И далее это свойство бы постепенно амплифицировалось. Вот это и был бы хороший пример появления нового фермента real-time."
Именно это и было сделано авторами. Был "некий исходный фермент" hisA S. enterica. Выращивая бактерий S. enterica в среде без триптофана, авторы отобрали бактерию-мутанта, у которой в результате двойной мутации (удвоение трех и замена еще одной аминокислоты)появилась "какая-то пусть и минимальная, но химическая активность по отношению к НОВОМУ для НЕГО (а не вообще для Земли :) типу субстрата". А именно, у фермента появилась "триптофановая" активность, которой исходно у данного фермента не было. И далее "это свойство постепенно амплифицировалось".
Утверждение комментатора, что в работе этого сделано не было, является прямой ложью.
-
А всё-таки мне не до конца понятно, какие выводы были сделаны из этих налюдений. По роду своей деятельности я далек от науки, но ваши исследования меня заинтересовали. По убеждениям я атеист, однако до этого не встречал мыслей, изложенных в этой работе. Хотелось бы понять, чтобы объяснили, для новичка, что именно произошло и под каким соусом нам это подают?
-
Затрудняюсь.
Во-первых, это не мои исследования, во-вторых, к атеизму или религии всё это не имеет прямого отношения. Дискуссия тут в комментах имеет отношение скорее к ошибкам в понимании (как науки, так и религии). В третьих, задача авторов здесь как раз в том и состоит, чтобы объяснять неспециалистам научные исследования. Если мне это не удалось - ну, значит, не удалось. Может быть, это просто не самый удачный выбор, с чего начать, если вы действительно новичок. А по ссылкам, данным в заметке, пробовали ходить? По ссылкам на другие заметки с Элементов, я имею в виду? Это в принципе должно помочь.
-
Александр Марков: ... в результате двойной мутации (удвоение трех и замена еще одной аминокислоты)появилась "какая-то пусть и минимальная, но химическая активность по отношению к НОВОМУ для НЕГО (а не вообще для Земли :) типу субстрата". А именно, у фермента появилась "триптофановая" активность, которой исходно у данного фермента не было.
...Утверждение комментатора, что в работе этого сделано не было, является прямой ложью.
=============================================
На самом деле фермент(ы) HisA/TrpF - изомеразы, которые катализируют одну и ту же реакцию Амадори: http://png-tm.ru/uplds/1351767031.png
Сокращенно обе реакции можно описать так:
альдоза-R <-> кетоза-R,
или даже, более специфично:
фосфоРИБОЗИЛ-формимино-арил <-> фосфоРИБУЛОЗИЛ-формимино-арил
где R - радикалы (арилы), которые отличаются в путях синтеза гистидина и триптофана. (у стрептомицетов и микобактерий даже есть родственный HisA фермент, PriA, катализирующий обе реакции с практически одинаковой Km)
Называть субстрат TrpF "новым типом субстрата", по сравнению с субстратом HisA - очень...громко сказано. Если только не считать ЛЮБОЙ субстрат - "отдельным типом". В любом случае, называть "прямой ложью" утверждение о том, что замена -R в альдоза-кетозной изомеризации не является "новым типом субстрата" - является БОЛЬШОЙ натяжкой.
А говорить о "триптофановой" активности у изомеразы HisA/TrpF - тоже натяжка, ("прямая ложь"? --конечно же нет, вообще "ложь" - это сознательная дезинформация, уверен, что ни Imperor, ни Марков _сознательно_ не лгут, чаще увлекаются, реже - ошибаются).
http://wiolowan.livejournal.com/1899.html
Эволюционные эксперименты
-
 17.03.2025Полногеномная дупликация дает немедленный адаптационный выигрышЕлена Наймарк • Новости науки
17.03.2025Полногеномная дупликация дает немедленный адаптационный выигрышЕлена Наймарк • Новости науки -
 23.03.2015Полиплоидия ускоряет эволюциюАлександр Марков • Новости науки
23.03.2015Полиплоидия ускоряет эволюциюАлександр Марков • Новости науки
-
 03.03.2015Ранние этапы адаптации предсказуемы, поздние — случайныАлександр Марков • Новости науки
03.03.2015Ранние этапы адаптации предсказуемы, поздние — случайныАлександр Марков • Новости науки
-
 30.06.2014Предсказуемый рост приспособленности достигается непредсказуемыми путямиАлександр Марков • Новости науки
30.06.2014Предсказуемый рост приспособленности достигается непредсказуемыми путямиАлександр Марков • Новости науки
-
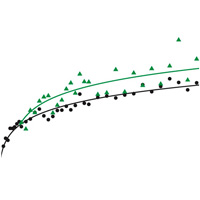 23.12.2013Новые результаты долгосрочного эволюционного эксперимента: приспособленность подопытных бактерий продолжает растиАлександр Марков • Новости науки
23.12.2013Новые результаты долгосрочного эволюционного эксперимента: приспособленность подопытных бактерий продолжает растиАлександр Марков • Новости науки
-
 23.10.2012Процесс появления новых ферментов прослежен в эволюционном экспериментеАлександр Марков • Новости науки
23.10.2012Процесс появления новых ферментов прослежен в эволюционном экспериментеАлександр Марков • Новости науки
-
 25.09.2012В долгосрочном эксперименте зафиксировано поэтапное формирование эволюционного новшестваАлександр Марков • Новости науки
25.09.2012В долгосрочном эксперименте зафиксировано поэтапное формирование эволюционного новшестваАлександр Марков • Новости науки
-
 01.02.2012Параллельная эволюция изучена в эксперименте на бактерияхАлександр Марков • Новости науки
01.02.2012Параллельная эволюция изучена в эксперименте на бактерияхАлександр Марков • Новости науки
-
 25.03.2011В долгосрочном эволюционном эксперименте выявлен отбор на «эволюционную перспективность»Александр Марков • Новости науки
25.03.2011В долгосрочном эволюционном эксперименте выявлен отбор на «эволюционную перспективность»Александр Марков • Новости науки
-
 01.11.2009Подведены итоги эволюционного эксперимента длиной в 40 000 поколенийАлександр Марков • Новости науки
01.11.2009Подведены итоги эволюционного эксперимента длиной в 40 000 поколенийАлександр Марков • Новости науки
Последние новости













Рис. 1. Бактерия Salmonella enterica. Изображение с сайта microbewiki.kenyon.edu