Читаем ДНК: в сто раз быстрее, в тысячу раз дешевле
Елена Клещенко
«Химия и жизнь» №1, 2006
Невидимые буквы
С тех пор как стало ясно, что за роль в нашей жизни играет ДНК, она остается в центре внимания мировой науки. Биохимики, биофизики, генетики, математики плечом к плечу двинулись на штурм двойной спирали. Ни один древний текст на мертвом языке, ни одну шпионскую радиограмму не расшифровывали с таким азартом. Ничего удивительного: наградой могут оказаться такие тайны, какие не снились археологам и контрразведчикам. Но и задача куда более сложная.
Алфавит составили сравнительно быстро, найдя соответствия между нуклеотидными триплетами и аминокислотами белков. Этот секрет людям выдали бактерии, которым подсовывали искусственно синтезированные матрицы, а потом наблюдали за процессом «чтения» — как если бы археолог мог попросить древнего египтянина прочесть вслух иероглифы, переписанные наугад. Сложнее со словарем: очень уж он велик даже у одного отдельно взятого многоклеточного, и нелегко установить значения всех разнообразных буквенных последовательностей, из которых состоит геном. Вдобавок лишь часть генома, кодирующая белки, записана известным нам триплетным кодом, в остальном же геноме действуют совсем другие правила. А еще, хотя триплетный «алфавит» практически одинаков у всех живых существ, «диалекты» могут так сильно различаться, что между родственными генами у эволюционно далеких видов трудно найти сходство без математических методов. Так что Далям и Ожеговым работы хватит надолго.
И еще одна незначительная деталь: генетическая информация не высечена в камне и не нанесена чернилами на пергамент, а представляет собой последовательность мономеров в биополимере. Простым глазом эти тексты даже не разглядишь. Приходится придумывать методы, по сравнению с которыми технические ухищрения гуманитарного цеха, вроде изучения палимпсестов в ультрафиолетовом свете, — просто милая забава.
Как было до сих пор
Дезоксирибонуклеиновая кислота, как и положено кислоте, в водном растворе дает анион. Если погрузить в раствор анод и катод, то фрагменты ДНК направятся к плюсу. Если вместо раствора будет гель на водной основе, то скорость фрагментов окажется обратно пропорциональной их длине: маленькие ниточки заскользят через гелевую сетку сравнительно быстро, а длинные будут чаще цепляться и ползти медленней. А поскольку пройденный путь, как известно, равняется скорости, умноженной на время, фрагменты ДНК, которые изначально находились в одной капельке смеси, через некоторое время выстроятся по росту. Метод электрофореза в геле применяется почти всегда, когда требуется рассортировать куски ДНК по длине, от большого к маленькому.
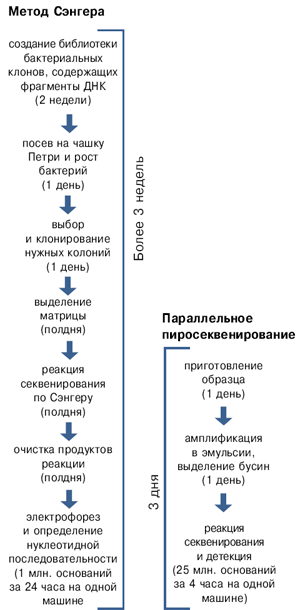
Высоковольтный электрофорез в полиакриламидном геле сделал возможным секвенирование по Сэнгеру — способ чтения ДНК, который оставался самым главным в течение десятилетий (первая публикация — 1977 год) и пока еще не превзойден по сочетанию простоты, точности и эффективности. Суть его в следующем: раствор фрагмента, назначенный к прочтению, разделяют на четыре части и в каждой части запускают реакцию полимеризации ДНК, в которой этот фрагмент играет роль матрицы. Помимо нормальных нуклеотидов в смесь добавляют и «тупиковые», обрывающие синтез цепочки, в каждую из четырех пробирок какой-нибудь один: А, Т, G или С. Количества реагентов и условия подбирают так, чтобы в каждой пробирке получились все возможные фрагменты: в первой — все, кончающиеся на А, во второй — на Т и так далее. А затем по капле из каждой пробирки помещают в лунки на геле и пропускают через него ток. Через некоторое время новосинтезированные кусочки ДНК разделяются по размеру, располагаясь узкими полосочками. Разумеется, простым глазом они не видны, но ученые выходят из положения, например, с помощью радиоактивной метки и рентгеновской пленки. Каждая полосочка соответствует одному нуклеотиду. На одной дорожке будут все буквы А, на другой — С и так далее, а по расстояниям от старта можно определить, какая буква за какой следует.
За прошедшие десятилетия метод Сэнгера был творчески развит и автоматизирован, а производство всех необходимых реагентов поставлено на широкую ногу. Другие методы, которые, казалось, могли представлять ему альтернативу (такие, как метод Максама — Гилберта, основанный на специфической деградации ДНК: читаемый фрагмент нарезали таким образом, чтобы получились все возможные куски с окончанием на определенный нуклеотид, а дальше опять-таки ставили электрофорез), не выдержали конкуренции. Зато из секвенирования по Сэнгеру выжали все возможное: как-никак столько геномов расшифровано, включая наш собственный. Но хочется читать ДНК еще скорее и дешевле, да притом без потери в точности. И ведь придется что-нибудь придумать — если мы действительно хотим заниматься медицинской генетикой, изучением биоразнообразия и тому подобными интересными вещами.
Папа и сын
С очередной попыткой создать технику быстрого чтения ДНК недавно познакомил своих читателей журнал Nature (2005, т. 437, с. 376–380). Новый метод секвенирования описали несколько десятков авторов под руководством Марселя Маргулиса и Майкла Эгхольма (Marcel Margoulies, Michael Egholm) из «454 Life Science Corporation» в Коннектикуте. (Кроме этой компании в работе участвовали Калифорнийский университет, Рокфеллеровский университет и Ротберговский институт детских болезней.)
Имя Джонатана М. Ротберга в списке авторов стоит последним, тем не менее новый метод уже называют «секвенированием по Ротбергу». И не просто так. Основатель корпорации «CuraGen», одной из ведущих компаний в области фармакогенетики, знаменит не только научными достижениями, но и тем, что регулярно попадает в списки самых молодых среди богатых и самых богатых среди молодых жителей планеты — сейчас ему чуть больше сорока лет. Однако разработка супербыстрого секвенирования была для него не только перспективным вкладом денежных средств.
Такие трогательные истории чаще происходят в голливудских научно-фантастических фильмах, но иногда случаются и в жизни. Шесть лет назад у Ротберга родился сын — и сразу же попал в отделение интенсивной терапии: мальчик не мог самостоятельно дышать. Отец не спал ночей от беспокойства, подозревая у ребенка генетическую болезнь. Молодые папы вообще склонны к панике, но доходы Ротберга позволяли ему паниковать с размахом. Он пообещал себе, что расшифрует весь геном сына.
Обещания обещаниями, но после проекта «Геном человека» всем известно, что это удовольствие стоит миллиарды долларов и занимает десятки лет. Столько Ротберг не мог ждать. Он основал «454 Life Science Corp.» и поставил перед ней задачу: создать такой метод чтения ДНК, какого еще не бывало. Чтобы немедленно и за реальные деньги — ну хотя бы миллионы, а не миллиарды...
Немедленно не получилось: понадобились годы. К счастью, здоровье Ротберга-младшего давно не внушает никаких опасений. Будет ли папа секвенировать его геном, неизвестно. Но в принципе такая возможность теперь есть.
С помощью нового метода можно прочесть 25 миллионов пар оснований (это весь геном низшего гриба) за четыре часа, а три миллиарда нуклеотидов, составляющих геном человека, — за сто дней, стоимость же такого проекта, по предварительным оценкам, составит всего-то около десяти тысяч долларов. Причем, в отличие от метода Сэнгера, для каждой реакции требуются не микролитры, а пиколитры раствора матрицы. Фактически дальше речь пойдет об отдельных молекулах!
Джеймс Уотсон, один из первооткрывателей двойной спирали, уже пообещал предоставить умельцам из Коннектикута образец своей крови, чтобы они подарили его генотип мировой науке и истории. (Не хуже, чем завещать собственный мозг родному институту! Даже интереснее, потому что даритель может сам поучаствовать в исследовании препарата...) О новом методе одобрительно отозвался и Дж. Крейг Вентер — еще один гигант молекулярной генетики, основатель института своего имени, президент знаменитой «Celera Genomics» (его статья, написанная совместно с Ю-Ху Роджерс, научным директором технологического центра при Институте Крейга Вентера, опубликована в том же номере «Nature»). В Институте Крейга Вентера тестировали новый метод секвенирования, так что слово двух этих ученых дорогого стоит. Не забыли они, впрочем, и указать на некоторые недостатки. Но сначала — о приятном.
Огоньки в сотах
Итак, берется образец ДНК, которую надо прочитать. Специальные ферменты нарезают его на кусочки случайным образом, и кусочки эти изолируют друг от друга предельным разведением. К каждому кусочку цепляют адапторную нуклеотидную последовательность, которая, в свою очередь, цепляется к маленькой бусинке (средний диаметр — 28 микрометров). К одной бусинке прикрепляется только один фрагмент. Затем бусины попадают в капельки водной эмульсии в масле. В этих капельках содержится все необходимое для амплификации ДНК методом полимеразной цепной реакции (ПЦР). Для чего нужна эмульсия и почему не подходит обычный водный раствор, объяснять не надо: каждая капелька — это отдельный реакционный сосуд, в котором копируется один и только один фрагмент ДНК. Как сказал журналистам сам Ротберг, при традиционном для метода Сэнгера клонировании фрагменты ДНК изолируют и наращивают в бактериальных клетках, а здесь роль клеток играют капельки эмульсии.
Здесь можно пофантазировать о лабораторном моделировании примитивных одноклеточных организмов. Масляное окружение водного пузырька с нуклеотидно-ферментным содержимым — чем не аналог липидной мембраны? Было бы слишком смело предполагать, что первые живые клетки возникли именно таким способом, поскольку на безжизненной Земле вряд ли нашлось бы нужное количество масла. Но тем, кто мечтает создать в пробирке новую форму жизни, стоит взять на заметку методику пиросеквенирования.
Однако вернемся к рутинной лабораторной работе. После ПЦР к каждой бусинке прицепляется около 10 млн. копий индивидуального фрагмента. Эмульсию разрушают, и бусинки, обросшие ДНК, центрифугированием загоняют в реакционные сосуды — открытые сверху микроскопические соты (диаметр каждой ячейки 44 микрометра, объем — 75 пиколитров). Соты размещены на волоконно-оптической подложке — квадратике размером 6 на 6 см, который несет на себе примерно 1,6 миллиона ячеек. Если бусина попадет не в каждый «колодец», это даже хорошо: меньше будет вероятность ложных сигналов.
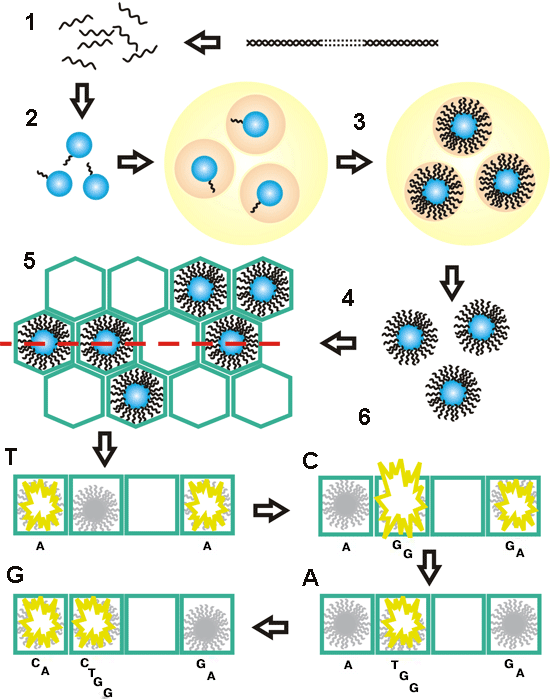
Теперь поместим пластинку в специальный прибор и будем омывать ее по очереди четырьмя растворами, содержащими нуклеотиды, — Т, С, A, G. Когда очередное основание присоединяется к цепочке, высвобождается пирофосфат и запускает флуоресценцию, поскольку в ячейках, помимо ДНК-полимеразы, присутствуют люцифераза и люциферин. Принцип этого метода — секвенирование методом синтеза, оно же пиросеквенирование или секвенирование в реальном времени, — впервые описал в 1988 году Эдвард Химан (Edward Hyman). Ферменты, как и ДНК, тоже прицеплены к бусинам, которые не вымываются из ячеек, а остаются на местах, как камешки на дне ручья, удерживая ферменты и матрицу, нуклеотиды же сменяют друг дружку. Пришел аденин — во всех сотах, где к цепочкам присоединяется А, вспыхивают огоньки, а остальные, ожидающие Т, G или С, остаются темными, пока не настанет их очередь. А дальше — дело техники. Оптические волокна передают вспышки на сенсорное устройство, компьютер записывает букву за буквой сразу в сотне тысяч последовательностей, а счастливый хозяин замечательного прибора заказывает пиццу, гуляет по интернету или расписывает всю эту методику для статьи в научном журнале — серьезно и подробно, а не как мы только что сделали.
Для публикации в Nature отсеквенировали геном бактерии Mycoplasma genitalium (580,069 н. п.). ДНК вредной инфекции нарезали на кусочки средней длиной 110 оснований, автоматизированная реакция (42 цикла по 4 нуклеотида) заняла всего 4 часа. Исследователи прочитали 96,5% генома микоплазмы с сорокакратным перекрыванием. Точность прочтения составила 99,96% (для апробации метода, естественно, выбрали уже известный геном, чтобы было с чем сравнивать). Удовлетворительные результаты были получены и с более крупным геномом Streptococcus pneumoniae (2,1 млн. н. п.).
Ложка дегтя
Во-первых, деньги. Прибор для секвенирования по Ротбергу стоит 500 000 долларов — не знаем, как для зарубежных лабораторий, а для россиян это сумма солидная. Да и реактивы требуются недешевые, и методика не самая простая. Хотя, конечно, с затратами на «Геном человека» не сравнить.
Во-вторых, секвенирование по Ротбергу позволяет читать только очень короткие фрагменты, максимум 120 нуклеотидов. При чтении более длинных кусков точность стремительно падает. А составлять из мелких кусочков огромный текст, например последовательность хромосомы млекопитающего, — удовольствие ниже среднего, особенно если учесть, что для высших организмов характерно обилие повторов. Вдобавок для пиросеквенирования нужны однонитевые кусочки ДНК, а не двунитевые, как при секвенировании по Сэнгеру, и, значит, можно забыть о комплементарных «липких концах», которые помогают состыковывать фрагменты. Придется повторять чтение по нескольку раз, с различными наборами перекрывающихся небольших кусочков, и потом собирать этот паззл с помощью хитроумных компьютерных программ.
В-третьих, у пиросеквенирования есть трудноустранимый дефект, причина которого лежит в самом принципе метода: когда в последовательности несколько раз повторяется одна и та же буква, не всегда получается определить, сколько же там Т подряд: семь или восемь. Об этом приходится судить по интенсивности вспышки, но здесь легко ошибиться. При секвенировании по Сэнгеру все гораздо понятнее: семь тиминов подряд — семь полосочек на соответствующей дорожке.
Однако все это, конечно, не отменяет несомненных достоинств метода (взгляните еще раз на таблицу, где он сравнивается с секвенированием по Сэнгеру). Скорее всего, оптимисты правы, и в самом деле уже настала эпоха быстрого чтения ДНК. Будущее покажет, победит ли этот метод или другой.
И немного о конкурентах
Не будем забывать, что у команды из Коннектикута есть серьезные соперники. Рядом с секвенированием по Ротбергу как бумажные, так и электронные издания регулярно упоминают полони-секвенирование (polony sequencing), которое придумала группа исследователей Гарвардской медицинской школы во главе с Джорджем Черчем (George Church). Исследователи обещают снизить стоимость чтения генома человека до 2,2 миллионов долларов, а в перспективе — даже до 1000 долларов.
Метод использует очень маленькие фрагменты ДНК, следовательно, лучше подходит для повторного чтения. Ничего обидного здесь нет: это означает, что метод Черча может быть применен и при секвенировании ДНК пациентов для медицинских целей (ведь геном человека уже прочитан), и, например, при изучении новых штаммов микробов. Золотое дно! Кстати, в Гарварде как раз и отсеквенировали геном новой линии кишечной палочки. Из оборудования потребовался обычный микроскоп с цифровой камерой. Название метода не связано ни с Польшей, ни с элементом полонием, а происходит от слов «polymerase colony» — «полимеразная колония». Десятки миллионов индивидуальных ДНК-фрагментов амплифицируются в тонком слое полиакриламидного геля. Поскольку гель ограничивает диффузию, образуются сферические колонии ДНК — полонии, говоря языком разработчиков. Они действительно напоминают бактериальные колонии в чашке Петри. (Опять ассоциации с искусственно созданной жизнью! Может, и вправду приближается время «полуживых механизмов»?) Затем двунитевую ДНК денатурируют, а на оставшихся однонитевых матрицах начинают сиквенс в реальном времени. Но по-другому, чем у Ротберга: к растущей цепи присоединяются флуоресцирующие аналоги нуклеотидов. Колония, присоединившая очередной нуклеотид, начинает светиться. Затем свечение нового нуклеотида гасят, отрывая и отмывая флуоресцентную группу. Повторяя циклы, фиксируя картинку камерой и передавая на компьютер, можно считывать последовательность сразу во всех этих миллионах точек. Правда, в каждой точке безошибочно прочитывается лишь очень короткий кусок, но точек-то миллионы! Так что поставленная задача — много, быстро, и дешево — выполняется неплохо.
Читая о ДНК в геле под микроскопом, светящихся метках и компьютерном анализе изображения, многие, наверное, вспомнили про аналогичные работы с ДНК-микрочипами академика А.Д. Мирзабекова и его коллег из Института молекулярной биологии в Москве. Спешу успокоить патриотов российской науки: разработчики полони-сиквенса в своих статьях на эти работы ссылаются. Конечно, все равно обидно — опять американцы в первых строчках новостей, а наши в середине списка цитируемой литературы. Но хочется верить, что еще не все потеряно.
-
Спасибо Елене Клещенко за прекрасный обзор. Как правило, популярные статьи грешат поверхностностью и безграмотностью, но эту статью я бы рекомендовал почитать всем, кто интересуется новыми веяниями в области секвенирования. Что касается отсутствия подобных российских разработок, то это правда, но "в действительности всё совсем не так, как на самом деле". Есть идеи, реализация которых позволит секвенировать геном человека примерно за неделю, причём на уже имеющемся оборудовании. Нужно только немного повозиться с биохимией. Проблема в том, что в России это никому не нужно.













