Глубины магматических океанов хватило для окисления мантии молодой Земли

Атмосфера молодой Земли сформировалась из газов, которые выделялись из ее мантии. Состав атмосферы и сейчас сильно связан с тем, что происходит в мантии. Важнейшим элементом для обеих оболочек является кислород, количество и форма нахождения которого определяют окислительно-восстановительные условия в них. До формирования металлического ядра и в мантии, и в атмосфере относительные концентрации кислорода были небольшими, но его обособление привело к окислению верхней мантии и изменению состава выделяющихся газов. По результатам экспериментов при давлениях и температурах, соответствующих разным глубинам силикатного магматического океана, покрывавшего Землю на ранних стадиях ее формирования, ученые из Баварского Геоинститута установили, что при этом происходит окислительно-восстановительная реакция с участием железа, которое при этом выделяется в чистой металлической форме и идет на рост ядра. Этот процесс, по мнению ученых, определил окислительно-восстановительные условия в мантии и привел к формированию алмазов из захваченного магматическим океаном CO2 из атмосферы.
Сразу после своего формирования, примерно 4,6 млрд лет назад, Земля не имела геологических оболочек — не было ни мантии, ни ядра, ни коры в современном понимании (рис. 2). Такое состояние молодых планет называется недифференцированным. Кора, мантия и ядро образовались позже, за счет плавления и разделения исходно более-менее однородного вещества планетезималей — процесса дифференциации. Важную роль в этом процессе сыграли магматические океаны, существовавшие в начале жизни Земли. За счет тепла от распада короткоживущих изотопов, а также постоянной метеоритной бомбардировки они не застывали на протяжении миллионов лет и имели глубину в сотни километров. Так как никто из ныне живущих ученых не видел магматического океана, предлагаются разные сроки их жизни: от 5 до 200 миллионов лет и даже дольше (L. Elkins-Tanton, 2008. Linked magma ocean solidification and atmospheric growth for Earth and Mars, Y. Abe, 1997. Thermal and chemical evolution of the terrestrial magma ocean).
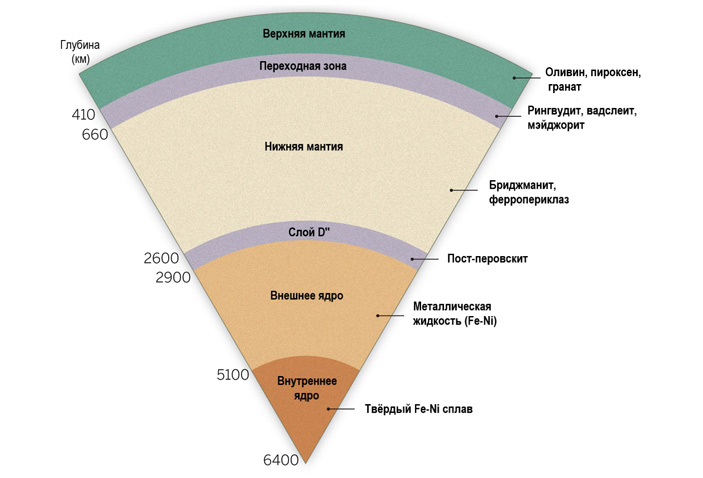
Рис. 2. Схематическое строение Земли и основные фазы, слагающие каждую из зон. Рисунок из статьи T. Sharp, 2014. Bridgmanite — named at last
Одним из главных результатов застывания магматического океана является мантия Земли, в основном состоящая из Mg-Fe-Si-O минералов, которые образовались из тонувших на дно оливинов и пироксенов (про почти аналогичный процесс, происходивший на Луне, можно почитать в новости На поверхности Луны обнаружен материал ее мантии, «Элементы», 13.06.2019).
Газы, выделяющиеся из магматического океана и формирующейся мантии, образовали первичную атмосферу Земли. Так как относительные содержания кислорода и там, и там были относительно низкими (примерно, как в исходных восстановленных планетезималях), набор газов был соответствующим: монооксид углерода (СО), метан (CH4) и водород (Н2). Если бы такой процесс дегазации продолжился без изменений до окончания кристаллизации магматического океана, то в итоговой атмосфере нашей планеты кислород бы отсутствовал из-за слишком восстановительной обстановки в мантии (D. Catling, M. Claire, 2005. How Earth's atmosphere evolved to an oxic state: A status report). Но, к счастью всех живых существ, уже на момент формирования первых горных пород мантия была окислена (см., например, D. Canil, 1997. Vanadium partitioning and the oxidation state of Archaean komatiite magmas). Однако, о самом механизме этого окисления до сих пор идет активная дискуссия и обсуждаемая статья предлагает достаточно элегантный вариант ее разрешения.
Поведение кислорода в геологических обстановках описывают с помощью фугитивности (fugacity) — аналога парциального давления газа с поправкой на неидеальность взаимодействий. Для описания окислительно-восстановительных условий в конкретной геологической среде, например, в верхней мантии или коре, пользуются минеральными буферами (рис. 3). Минеральные буферы (mineral redox buffer) — это химические реакции, задающие определенную фиксированную фугитивность кислорода, так что можно говорить об отклонении от них в ту или иную сторону.
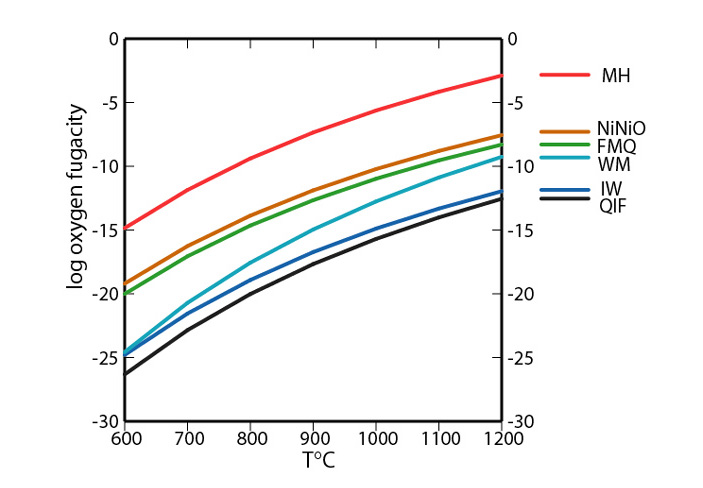
Рис. 3. Различные буферные реакции и задаваемые ими фугитивности при давлении в 1 бар (MH — магнетит/гематит, NiNiO — Ni/NiO, FMQ — фаялит/магнетит/кварц, WM — вюстит/магнетит, IW — железо/вюстит, QIF — кварц/железо/фаялит). Рисунок с сайта wikipedia.org
Для мантии часто используется буфер железо (Fe) — вюстит (wüstite, FeO):
2Fe + O2 = 2FeO.
При условии, что вюстит и железо не содержат примесей других элементов, константа равновесия реакции запишется как:
\[\mathrm{К}_{\mathrm{р}}=\dfrac{1}{f_{\mathrm{O}_2}}.\]где \(f_{\mathrm{O}_2}\) — фугитивность. Логарифмируя обе части, получаем:
\[-\log{\mathrm{К}_{\mathrm{р}}}=\log{ f_{\mathrm{O}_2}}.\]Основным из предложенных ранее механизмов окисления мантии была реакция с участием воды (H2O), в результате которой кислородные фазы оставались в мантии, а водород выделялся и диссипировал в космическое пространство (J. Kasting et al., 1993. Mantle Redox Evolution and the Oxidation State of the Archean Atmosphere). Эта реакция совершенно точно происходила, но вопрос о том, хватило ли Земле воды на окисление всей мантии после формирования ядра, остается открытым. Этой гипотезе противоречит также то, что более богатый летучими компонентами Марс имеет более восстановленную мантию (см., например, C. Herd et al., 2002. Oxygen fugacity and geochemical variations in the martian basalts: implications for martian basalt petrogenesis and the oxidation state of the upper mantle of Mars).
Альтернативой водному окислению является процесс диспропорционирования FeO (окислительно-восстановительная реакция, в которой железо является и окислителем, и восстановителем):
3Fe2+O = Fe3+2O3 + Fe0.
Оно происходит, к примеру, при кристаллизации бриджманита (bridgmanite — MgSiO3 со структурой перовскита), главного минерала нижней мантии (D. Frost et al., 2004. Experimental evidence for the existence of iron-rich metal in the Earth's lower mantle). Это означает, что при формировании нижней мантии реакция смещалась вправо, что приводило к выделению чистого железа. Оно, в дальнейшем, тонуло и входило в состав ядра, в результате чего над восстановленным металлическим ядром получалась достаточно окисленная мантия.
Изучив эту же реакцию в силикатном расплаве при давлениях до 23 ГПа и температурах до 2473 К, ученые из Баварского Геоинститута установили, что существует еще один механизм, который может привести к окислению мантии: они выяснили, что диспропорционирование в глубине силикатного магматического океана происходит без участия бриджманита. Результаты работы опубликованы в недавнем выпуске журнала Science.
Если Fe2+ и Fe3+ присутствуют в силикатном расплаве, выражение для фугитивности запишется так:
4FeO + O2 = 2Fe2O3.
Чтобы упростить последующие расчеты, все коэффициенты реакции можно поделить на 4, соотношение элементов от этого не изменится:
FeO + 1/4O2 = FeO1,5.
\[ f_{\mathrm{O}_2}=\left(\dfrac{a^{\mathrm{распл}}_{\mathrm{FeO}_{1{,}5}}}{ a^{\mathrm{распл}}_{\mathrm{FeO}}\cdot K}\right)^4,\]где К — константа равновесия этой реакции, а буквой a с индексами обозначена активность соответствующих соединений. При нормальном давлении К такова, что силикатный расплав в равновесии с Fe0 почти не содержит Fe2O3. Чтобы его количество возросло при увеличении давления, объемный эффект реакции ΔV = VFeO1,5 − (VFeO + 1/4VO2) должен быть отрицательным.
Таким образом, для того, чтобы определить знак ΔV, была поставлена серия экспериментов с силикатным расплавом, содержащим железо (рис. 4). Расплавы андезитового состава при постоянном давлении и с фугитивностью на уровне буфера Ru-RuO2 (+8 log-единиц относительно буфера Fe-FeO) закаливались в стекла с разных температур. В полученных стеклах с помощью мессбауэровской спектроскопии определялось отношение Fe3+/ΣFe. В предыдущих работах, в которых давление доходило до 7 ГПа, получался положительный ΔV, то есть предпочтительным было существование трехвалентного железа, что вполне соответствует известным давлениям и сжимаемостям при атмосферном давлении. Однако, как сейчас выяснилось, при увеличении давления на отметке 10 ГПа тренд меняется на противоположный: Fe3+/ΣFe начинает возрастать. Авторы предполагают, что такой эффект наблюдается из-за большей чем у FeO сжимаемости Fe2O3 в расплаве, что, в свою очередь, является следствием изменения координации Fe3+ (то есть расположения атомов кислорода и кремния вокруг атома железа).
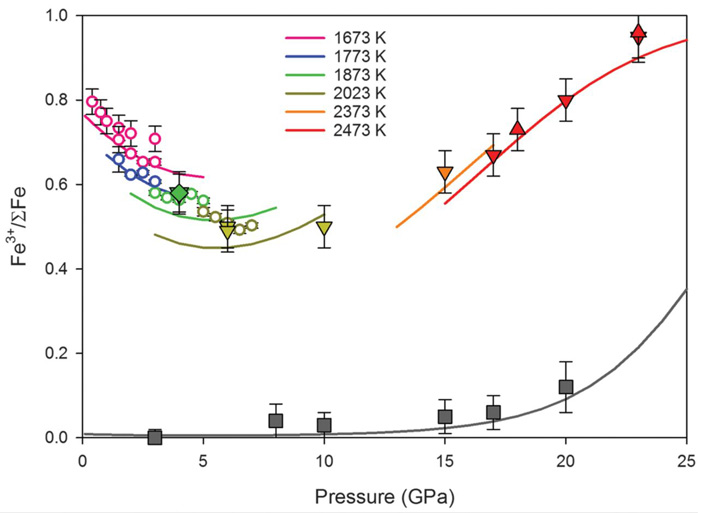
Рис. 4. Доля трехвалентного железа в закаленном расплаве при различных давлениях и температурах. График из обсуждаемой статьи в Science
Полученные в ходе эксперимента данные были подставлены в термодинамическую функцию, описывающую зависимость Fe3+/ΣFe в расплаве от температуры, давления фугитивности кислорода и состава расплава, и на их основе был произведен аппроксимационный расчет термодинамических коэффициентов (H. O’Neill et al., 2006. An experimental determination of the effect of pressure on the Fe3+/∑Fe ratio of an anhydrous silicate melt to 3.0 GPa; K. Jayasuriya et al., 2004. A Mössbauer study of the oxidation state of Fe in silicate melts). Для описания объемов фаз использовались модифицированные уравнения Тейта третьего порядка. Эта модель хорошо описывает экспериментальные данные и показывает, что ΔV, определяющий Fe3+/ΣFe, не зависит от fO2. При этом увеличение стабильности Fe2O3 при возрастающем давлении означает увеличение реальной доли этого соединения в расплаве в равновесии с металлическим железом (Fe0). Это значит, что из расплава, почти не содержащего Fe2O3, в условиях с давлением более 10 ГПа будет выделяться металлическое железо, необходимое для баланса с Fe2O3, возникшего из FeO.
На планетах земного типа и малых телах на ранних стадиях формирования существовали силикатные магматические океаны разной глубины. Использовав свою модель, авторы построили график зависимости окислительных условий от глубины океана и Fe3+/ΣFe (рис. 5). Гипотетический первичный магматический восстановленный океан, в котором металлическое железо стабильно на поверхности, имеет Fe3+/ΣFe около 0,004. До глубины 200 км насыщение металлом снижается, а потом начинает возрастать до 400 км, где металлическое железо снова стабильно и возможна реакция диспропорционирования.
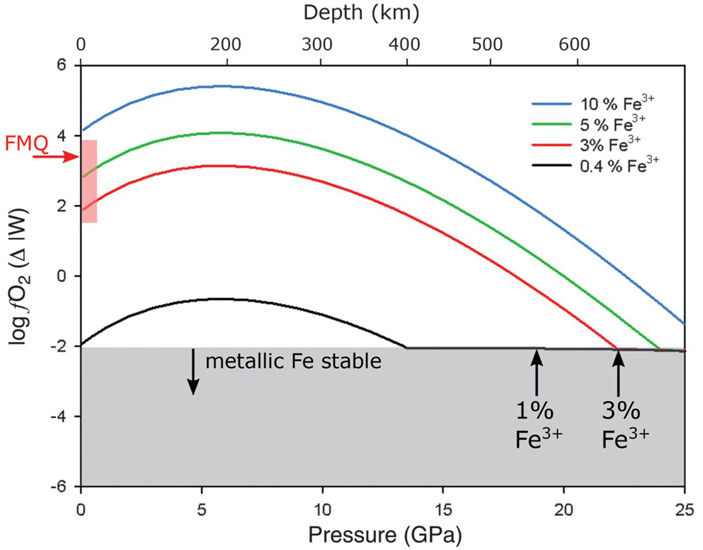
Рис. 5. Профили фугитивности в магматическом океане в зависимости от содержания железа. График из обсуждаемой статьи в Science
Если получившееся железо (Fe0, в форме капель металла) тонет к ядру, то доля Fe3+ в силикатном расплаве возрастает . При удалении 0,1 весового процента металла с одновременной гомогенизацией за счет конвекции отношение Fe3+/ΣFe составит 0,03, что сходится с оценками для современной мантии Земли. Более того, получающееся изменение фугитивности с глубиной соотносится с существующими профилями для мантии (D. Frost, C. McCammon, 2008. The Redox State of Earth's Mantle). Так, факт возникновения металлического железа на модельных глубинах подтверждается находками включений железного расплава в алмазах с глубин 400–660 км (E. Smith et al., 2016. Large gem diamonds from metallic liquid in Earth’s deep mantle). Более того, диспропорционирование может объяснить то, что на Марсе, Луне и Весте мантии восстановленные: глубины магматического океана на них просто не хватало для достижения давлений, необходимых для протекания реакции.
Наличие градиента фугитивности в магматическом океане приводит к возникновению так называемого «углеродного насоса» (M. Hirschmann, 2012. Magma ocean influence on early atmosphere mass and composition). Это механизм, который постоянно забирает немного CO2 из атмосферы за счет растворения в магме и запасания в мантии в форме алмазов. Его роль была особенно большой после катастрофического столкновения, которое, вероятно, случилось, когда Земля только сформировалась, и привело к формированию Луны: это объясняет, почему значительная часть углерода Земли находится в мантии, а водорода и азота — преимущественно в атмосфере. При Fe3+/ΣFe = 0,03, по подсчетам авторов, из-за снижения фугитивности кислорода растворенный CO2 в расплаве начнет выпадать в форме алмаза на глубинах около 500 км.
Предложенный авторами механизм окисления мантии не только решает ряд противоречий предыдущих гипотез, но и позволяет объяснить некоторые дополнительные явления, тем самым претендуя на роль новой основной гипотезы в этом вопросе.
Источник: Katherine Armstrong, Daniel J. Frost, Catherine A. McCammon, David C. Rubie, Tiziana Boffa Ballaran. Deep magma ocean formation set the oxidation state of Earth’s mantle // Science. 2019. DOI: 10.1126/science.aax8376.
Кирилл Власов
-
Это полный ппц, блджад!
Такое ощущение, что эти люди с Луны свалились да и до сих пор живут в своём вакуумном манямирке, не видя и не зная, что делают другие (более адекватные) камрады... :(
Рисунок 4 напрямую противоречит всему их словоблудию (и здравому смыслу): чем глубже, тем больше температура/давление и.. больше окисленного железа. Та-дам! Рукалицо.
Прямая через одну точку... Рукалицо.
Вогнутая кривая через две (с половиной) точки... И даже через одну! Fuuuuuuuu -
-
Без химических формул тут просто ничего будет непонятно, а термодинамические формулы нужны для хоть какого-то объяснения главного понятия в статье (фугитивности). Там про него в начале простое объяснение, а потом посложнее - с формулами (которое можно опустить, если не важно). Резюмируя - можно написать без формул, но тогда что конкретно сделали объяснить вряд ли выйдет, только выводы (примерно как в первом абзаце). Но статья сложная вышла для чтения, совершенно согласен.
-
Поэты позавидуют верности этих слов!)
Смутила нестройность решения популяризаторской задачи:
То подробно объяснено сохранение равенства при делении обеих сторон его на 4 (начальная школа),
То фугитивность упомянута без даже намека на ее смысл (сколько помню, и в старших классах школ не упоминаемая)
И про формулы, правда, как-то неоправданно - многие тут обстоятельства, которые эти формулы должны разъяснять, ощутимо проще, экономнее, яснее было бы выразить словами - буквально парой-тройкой)
А в целом -оч интересно.
Если б уважаемый Антихимик не обратил внимание на неубедительность графиков -еще бы лучше было!)
-
То фугитивность упомянута без даже намека на ее смысл
Ну не совсем уж так, там про неё и её смысл два абзаца с графиком и теми самыми страшными формулами. Но, видимо, объяснительный эффект формул не очень получился и надо добавить перед всеми этими штуками абзац с максимально упрощенным объяснением понятия, чтобы суть статьи была доступнее. Я сейчас так и сделаю.Если б уважаемый Антихимик не обратил внимание на неубедительность графиков
Вот мне всегда очень сложно отвечать на комментарии, которые пишутся таким языком и с такими обвинениями в адрес статьи в Science. Потому что не ясно - то ли ты плохо объяснил и человек просто не понял механизма и про что график (тут я всегда рад объяснить ещё и исправиться), то ли это просто комментарий ради комментария, выплеснуть эмоции и пойти дальше. Но раз уж вопрос снова возник - четвертый график абсолютно правильный и ничем статье не противоречит. Он не про Землю и любые планеты в целом, он конкретно про магматический расплав (который лишь часть магмы, там кроме него ещё кристаллы минералов и флюидная фаза). Базальтовый расплав и горные породы современной мантии это совершенно разные вещи и процесс диспропорционирования, который происходит в расплаве в породах не произойдет (и не происходит, породы и их составные части мы давили до гораздо больших давлений). Да, в расплаве вот столько Fe3+, но там же ещё вместе с ним рядом капельки Fe0 плавают. И только после их удаления степерь окисления магмы и образующейся из неё породы изменится. А до этой статьи вообще не было известно что происходит с железом в расплаве при таких давлениях и температурах, это самые новые последние данные.-
четвертый график абсолютно правильный и ничем статье не противоречит
Оооокей...
Ещё раз (и подробно):
1. Если вы обратитесь к Table S5 (p.33-34), то можете заметить, что Fe(0) присутствует лишь в "нижних" образцах (S6729, S6665, Z1626, Z1647), т.е. тех, что эмулировали восстановленное железко и нанесены в виде серой кривой на Рис.4. Fe(0) исключалось из калькуляции "суммарного" содержания железка (p.5).
2. Если вы подниметесь чуть выше к Table S4 (p.32), то среднее "суммарное" содержание железка в андезитовых образцах составляет ок. 7,5+/-0,9; в морбовых образцах - ок. 8,3+/-0,9; и в восстановленных образцах - ок. 12,8+/-1,2. (NB! Статистически значимой разницы между андезитовыми и морбовыми образцами нету.)
3. Теперь возвращаемся к Рис.4: до ~10 ГПа доля Fe(3+) потихоньку снижается, стабилизируется, а затем (с ~15 ГПа) начинает расти. Отвод в Fe(0) тут не роляет (см. п.п.1-2).
Так чем же отличается область до 10 ГПа и после 15 ГПа? Температурой. После 15 ГПа температуру увеличили от 1900 до 2100-2200 гр.Ц.
Интересно, что восстановленные образцы с такой же увеличенной температурой (точки 15, 17 и 20 ГПа, Table S2, p.30) дают идентичный (!!) тренд на увеличение доли Fe(3+).
Однако ж авторы делают "внезапный" вывод про сжимаемость и координацию железка... Шта??!
Я бы так не возмущался, если бы авторы хотя бы были последовательны и бОльшее внимание уделили физ.-хим. процессам при повышенных температурах, а не вот так вот - пальцем в носу. Фугитивность, вот тож, зачем-то приплели... :)-
Спасибо, так гораздо понятнее - я сразу даже не смог разобрать, какая часть статьи вас возмутила) Понятно, что основной источник информации здесь - 5 экспериментов, сделаных при 2473 К. Ну и один на 2373, чтобы показать что похож. Тут ключевой момент, что фугитивность буферирована, температура постоянна, следовательно на изменение отношения влияют меняющиеся свойства расплава при увеличении давления. Скопипащу просто кусок статьи:
"At ambient pressure, K is such that silicate melts in equilibrium with metallic iron contain negligible Fe2O3. For this to change at higher pressures, the volume change for Eq. 1, dV must be negative. We can determine the sign of dV by examining whether the Fe3+/Fe (total) ratio of a silicate melt increases with pressure at a constant temperature and buffered oxygen fugacity."
Если вы считаете, что там есть какие-то внезапные redox процессы при буферированной фугитивности, то поделитесь, ну или ссылку хоть на более прогрессивных товарищей. Поймаю кого-нибудь из авторов статьи в коридоре, расскажу, напишем вместе ещё одну статью в Science)))
Понимаю, что принципиально возмущает момент, что при малых давлениях меньше температура, а при больших - бОльшая. Но это обусловлено геологической обстановкой, те же эксперименты можно сделать при меньших Т, но это будут условия не соответствующие реальным. Конечно же хотелось бы видеть для каждой Т непрерывную линию от 1 до 25 ГПа, но это будущая работа, сейчас - первые самые новые данные. "Застолбили", так сказать. Что же касается интерпретации экспериментальных данных - я с ней согласен и полагаю, что будущие работы (как раз с непрерывными кривыми для одной Т) не изменят серьезно выводов и общего механизма.
P.S. Я с вашим комментарием полностью согласен, всё верно, в экспериментах нет удаления железа и сопряженного окисления, там всё забуферировано наглухо) Писал про этот механизм потому что не очень понял какой из моментов вам был не ясен.-
At ambient pressure, K is such that silicate melts in equilibrium with metallic iron contain negligible Fe2O3. For this to change at higher pressures, the volume change for Eq. 1, dV must be negative. We can determine the sign of dV by examining whether the Fe3+/Fe (total) ratio of a silicate melt increases with pressure at a constant temperature and buffered oxygen fugacity.
Прям как казахские акЫны - чего вижу то пою... :]Если вы считаете, что там есть какие-то внезапные redox процессы при буферированной фугитивности, то поделитесь
Я человек далёкий. Грамотами и регалиями не увешан. :D
Но по моему скромному мнению...
1. Надоть обратить внимание на температурные фазовые переходы (см. Table S3). В стеклообразном состоянии процесс идёт, как положено/предполагается; а в кристаллических - абы как. Это жжжжжжжж неспроста.
2. Надоть протянуть зависимости для 2173К вверх до 20-25 ГПа, а для 2373-2473К вниз до н.у.
3. Очень много оксида рутения залазит в крист.фазу при повышенной температуре/давлении (Table S3, S4). Это нужно решать. Скорость нагрева/охлада?..
(4). Возможный(е) артефакт(ы) методики? Можно ли определить железко непосредственно в ячейке?..
-
-
-
Ключевая физхимия "для школьников" тут описывается в рамках принципа Ле Шателье: повышенная сжимаемость Fe2O3 смещает равновесие в сторону этого компонента при повышенном давлении, при этом дополнительно запускается "осаждение" из равновесной системы железа, что еще сильнее смещает равновесие в сторону Fe + Fe2O3.
Интересно, следует ли из всего этого, что мантия Луны должна быть более богата железом?
Последние новости




См. также















Рис. 1. Молодая планета на стадии магматического океана. Рисунок с сайта forbes.com