Гидросульфид и сероводород в гидротермальных растворах способствуют формированию месторождений золота
Крупные промышленные месторождения золота часто формируются при участии гидротермальных водных растворов, содержащих значительные концентрации серы. Долгое время ведется дискуссия относительно того, в какой химической форме сера присутствует в таких растворах, так как растворимость золота и других металлов напрямую зависит от типа образующихся комплексных соединений. Многие ученые настаивают на том, что на роль главных форм нахождения серы в растворах лучше всего подходят S6+, S2− и S3−. Однако новые эксперименты небольшой команды из Университета Женевы с использованием аппарата, позволяющего точно контролировать окислительно-восстановительные условия, указывают на то, что скорее всего сера присутствует в виде гидросульфида (HS−), сероводорода (H2S) и SO2. Это означает, что в восстановленных магматических гидротермальных растворах золото более склонно к образованию комплексов с HS− и H2S, значительно улучшающими растворимость металла, что имеет важные последствия для понимания механизмов его транспорта и концентрации.
Гидротермальные водные растворы, которые геологи называют флюидами (ударение на «ю»), играют важную роль в формировании ряда месторождений критически важных металлов, таких как медь, серебро или золото. Вообще, флюиды бывают самые разные, но на глубинах около 5 километров они обычно состоят из смеси H2O, CO2 и различных растворенных в них химических элементов. В основном это щелочные и щелочноземельные металлы, галогены, сера, в меньшей мере — кремний и алюминий. Также во флюидах можно найти значительную часть таблицы Менделеева, в том числе золото, медь и серебро, однако обычно в достаточно небольших концентрациях — порядка сотен грамм на тонну или меньше.
Флюиды чаще всего образуются в результате дегазации магмы, так как растворимость H2O или CO2 в магматическом расплаве уменьшается при подъеме к поверхности (подробнее про это см. картинку дня Уникальные минералы Камчатки и статью Глубинное кипение магмы). В образующийся при дегазации раствор из магмы переходит значительное количество серы, хлора, калия, натрия, а также различных металлов, предпочитающих флюидную фазу расплаву. При этом еще недавно растворенная в магматическом расплаве вода сама становится растворителем. По трещинам в земной коре такие растворы мигрируют в более холодные удаленные от магматического тела зоны, где и образуются рудные минералы.
Если ограничиваться качественным описанием, то описанная схема формирования месторождений металлов достаточно простая и понятная. Проблемы начинаются при попытке выяснить детали: например, сколько именно золота может растворяться в таком флюиде, в форме каких химических комплексов, ионов или соединений оно там присутствует и как на все это влияет изменение давления, температуры или окислительно-восстановительной обстановки. Дело в том, что металлы в гидротермальных растворах очень редко существуют в форме свободных ионов или коллоидных частиц, они как правило образуют комплексы и сложные ионы с другими растворенными элементами. Тип комплекса или иона сильно влияет на растворимость металла и зависит от ряда параметров, таких как химический состав раствора, давление и температура. Это делает точное определение формы нахождения золота в растворе важной, но весьма трудоемкой задачей.
В связи с критическим значением золота для мировой экономики эта задача уже долгое время находятся в центре внимания множества научных групп по всему миру. Достаточно давно известно, например, что золото хорошо растворяется во флюидах в форме хлоридных комплексов вроде Au(Cl)2− и Au(Cl)4− в достаточно широком диапазоне давлений и температур. Хлор является одним из самых распространенных элементов во флюидах (C. Manning, 2018. Fluids of the Lower Crust: Deep Is Different), но большую роль в транспорте металлов играют и другие элементы, особенно сера. Термодинамические расчеты и ряд пилотных экспериментов указывают на то, что многоатомный ион Au–HS− может быть более стабилен чем Au(Cl)2− на глубине нескольких километров (J. Brugger et al., 2016. A review of the coordination chemistry of hydrothermal systems, or do coordination changes make ore deposits?), однако однозначного экспериментального подтверждения этому факту не было. Более того, некоторые ученые склоняются к тому, что такие ионы как S2− и S3− могут играть более важную роль чем HS− , что подтверждается термодинамическими расчетами и экспериментами (см., например, статьи G. Pokrovski et al., 2015. Sulfur radical species form gold deposits on Earth; G. Pokrovski, J. Dubessy, 2015. Stability and abundance of the trisulfur radical ion S3− in hydrothermal fluids; G. Pokrovski et al., 2022. Gold speciation in hydrothermal fluids revealed by in situ high energy resolution X-ray absorption spectroscopy).
Причина такого разногласия кроется в том числе в высокой технической сложности экспериментов, которые могли бы его разрешить. Чем выше температура и давление, тем сложнее контролировать условия и обеспечить чистоту состава, особенно в случае с крайне химически активными флюидами. Особенно тяжелой задачей оказался контроль за окислительно-восстановительной обстановкой — параметром известным среди петрологов-экспериментаторов как фугитивность кислорода (подробнее см. Глубины магматических океанов хватило для окисления мантии молодой Земли, Элементы, 12.09.2019).
Чаще всего в экспериментальной геохимии окислительные или восстановительные условия обеспечиваются за счет использования увлажненной буферной смеси химических соединений (рис. 2), отделенной от образца проницаемой для водорода мембраной, такой как стенка платиновой капсулы. Однако наличие такой капсулы делает невозможным использование главного метода изучения высокотемпературных комплексов золота — рентгеновской абсорбционной спектроскопии (X-ray absorption spectroscopy): платина слишком хорошо поглощает синхротронное излучение. При этом рассчитать фугитивность кислорода на основе чисто термодинамических соображений тоже вполне возможно и это будет допустимая и достоверная оценка, однако расчет параметра и его контроль в эксперименте — принципиально разные подходы.
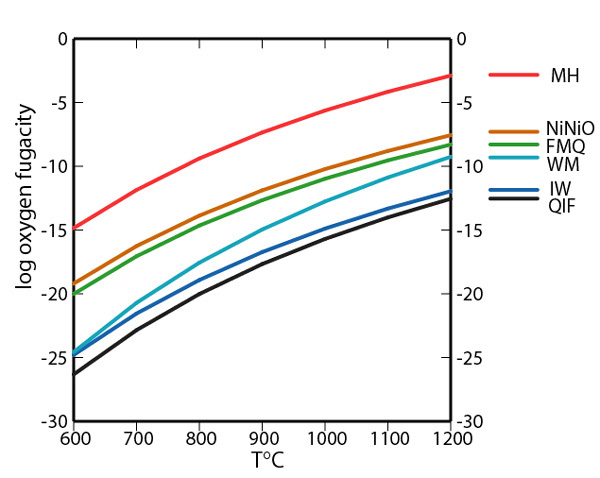
Рис. 2. Фугитивность кислорода, контролируемая смесями различных минералов при давлении в 1 бар — от более окислительных (красный) до более восстановительных (черный). MH — магнетит/гематит, NiNiO — Ni/NiO, FMQ — фаялит/магнетит/кварц, WM — вюстит/магнетит, IW — железо/вюстит, QIF — кварц/железо/фаялит. Обратите внимание, что все значения в обсуждаемой статье даны в относительных единицах отклонений от расчетного значения NiNiO при температуре 875°C и давлении 2000 бар, то есть не соответствуют этому графику. Рисунок с сайта wikipedia.org
Здесь нужно отметить, что в случае использования буферов или иных способов контроля фугитивности кислорода мы на самом деле контролируем фугитивность водорода, которая в свою очередь смещает баланс реакции 2H2O = 2H2 + O2 в ту или иную сторону. Таким образом, наиболее тонкий контроль окислительно-восстановительных условий достигается в аппаратах, где есть возможность напрямую устанавливать парциальное давление водорода, находящегося в контакте с изучаемым образцом флюида.
Именно такую установку и построил один из авторов обсуждаемого исследования, Золтан Заяц (Zoltan Zajacz), в Университете Женевы. В ее основе достаточно популярный метод, в котором для поддержания высокого давления и температуры в эксперименте используются металлические автоклавы, помещенные в муфельную печь (см. Cold Seal Pressure Vessels). Золтан Заяц и его студенты в прошедшие годы усовершенствовали этот дизайн, добавив к нему специальную мембрану. Она позволяет создавать внутри молибден-гафний-карбидного (MHC) автоклава аргон-водородную атмосферу заданного состава и точно контролировать фугитивность кислорода. Это дало им возможность задавать параметры, отличные от фиксированного значения минерального буфера: от −0,9 до +2,6 относительно значения NiNiO при температуре и давлении эксперимента.
В статье, недавно опубликованной в журнале Nature Geoscience, Штефан Фарсанг (Stefan Farsang) и Золтан Заяц представили новейшие данные относительно стабильности комплексов серы и растворимости золота в гидротермальных флюидах, полученные с помощью описанной установки. Так как данный автоклав не позволяет анализировать флюид in situ прямо во время эксперимента, авторы применили метод синтетических флюидных включений (рис. 1, 3). В этом методе используется свойство кристаллов захватывать растворы и расплавы при залечивании трещин, образуя своеобразные аналитические микроампулы (рис. 3, d).

Рис. 3. a — фотография и схема золотой капсулы, использовавшейся в экспериментах (Au capsule — золотая капсула, quartz cylinder — цилиндр, выпиленный из кристалла кварца, aqueous solution — водный раствор, silica gel — силикагель); b — две экспериментальные установки: на левой муфельная печь открыта, на правой автоклав установлен в экспериментальной позиции; c — поперечный спил кварцевого цилиндра с захваченными включениями после эксперимента; d — включения флюида в кристалле кварца; e — нагревательная установка для анализа включений после эксперимента, помещенная под рамановский микроскоп. Изображение из обсуждаемой статьи
Авторы подготовили цилиндры, вырезанные из кристалла кварца, подвергли их термальному шоку для образования трещин и поместили в специальную капсулу вместе с раствором, имитирующим состав серосодержащего хлоридного магматического флюида (рис. 3, а). На дно капсул был добавлен аморфный кремнезем, который во время эксперимента ускорял залечивание трещин и захват образцов флюида внутри кварца. Капсула помещалась в MHC-автоклав, который подключался к газораспределительной системе и устанавливался в муфельную печь (рис. 3, b). Экспериментальные параметры соответствовали высокотемпературной гидротермальной системе, сопутствующей магматической интрузии на глубине около 6–7 км (2000 бар, 875°C). После эксперимента, кристаллы кварца извлекались из капсулы распиливались на пластины, а захваченные включения анализировались с помощью спектроскопии комбинационного рассеяния (СКР) и масс-спектрометрии с индуктивно-связанной плазмой (LA-ICP-MS).
Так как кварц — минерал достаточно прочный, давление внутри флюидных включений соответствовало экспериментальному, а вот для достижения необходимой температуры при спектроскопических измерениях пластины поместили в специальную мини-печку (рис. 3, е), помещающуюся под рамановский микроскоп. Такой вторичный нагрев необходим для того, чтобы изучить высокотемпературные ионы и соединения, нестабильные при комнатной температуре. Так как давление и фугитивность кислорода внутри включения уже полностью соответствует экспериментальному, нагрев позволяет окончательно вернуть флюид в «исходное» состояние. Одним из важных новшеств авторов было использование коротковолнового лазера с длиной волны 405 нм, позволявшего получать спектры высокого разрешения даже при максимальной температуре (875°C) за счет минимизации термального бэкграунда. Тонкий контроль за фугитивностью кислорода и выдающееся качество спектров позволили определить, в какой именно форме сера присутствует в окисленных или восстановленных флюидах на глубине 5–6 километров (рис. 4, 5).

Рис. 4. Рамановские спектры включений, захваченных при восстановительных (a, b) и окислительных (c, d) условиях, полученные при их нагреве после эксперимента. Обратите внимание на то, какие соединения и ионы серы наблюдаются при температуре 875°C (b, d) и сравните тем, что видно при комнатной температуре (a, c). Высота пика пропорциональна концентрации иона или соединения: в восстановительных условиях это почти полностью HS− и H2S (b, выноски), а в окислительных — SO2 (d, выноски). Host quartz — референсный спектр кристалла кварца, liquid — жидкая фаза, vapour — газообразная фаза; Entrapment — условия захвата включения. Графики из обсуждаемой статьи
Результаты описанных экспериментов расходятся с рядом существующих гипотез и моделей (рис. 5, b, c), указывая на то что скорее всего сера встречается в виде HS− и H2S (с небольшой примесью H2Sn) в восстановительных условиях и в виде SO2 в окислительных. Авторы также указывают на то, что использование лазера с длиной волны 405 нм позволяет избежать резонанса с энергетическими уровнями S2− и S3−. Эти формы нахождения серы действительно хорошо заметны на спектрах включений при использовании лазера с длиной волны 532 нм, однако исчезают если использовать 405 нм источник излучения. На основе этого и анализа энергетических уровней этих ионов, авторы полагают что роль S2− и S3− в гидротермальных растворах была в прошлом переоценена из-за некорректной интерпретации спектров, в которых высокая интенсивность возникала не из-за повышенных концентраций, а благодаря эффекту резонанса.

Рис. 5. a — преобладающие ионы и соединения серы в гидротермальных растворах на основе экспериментов авторов статьи; b, c — преобладающие ионы и соединения серы по версии двух других моделей из литературы. Вертикальная ось — мольные доли от общего бюджета серы, горизонтальная ось — фугитивность кислорода в отклонениях от значения буфера NiNiO при 2000 бар и 875°C. Графики из обсуждаемой статьи
Для оценки влияния окислительно-восстановительных условий на растворимость золота в серосодержащих гидротермальных флюидах авторы также проанализировали концентрации Au во включениях с помощью LA-ICP-MS. Все эксперименты проводились в золотых капсулах, то есть растворы были насыщенные, и авторы измеряли максимально возможные концентрации.
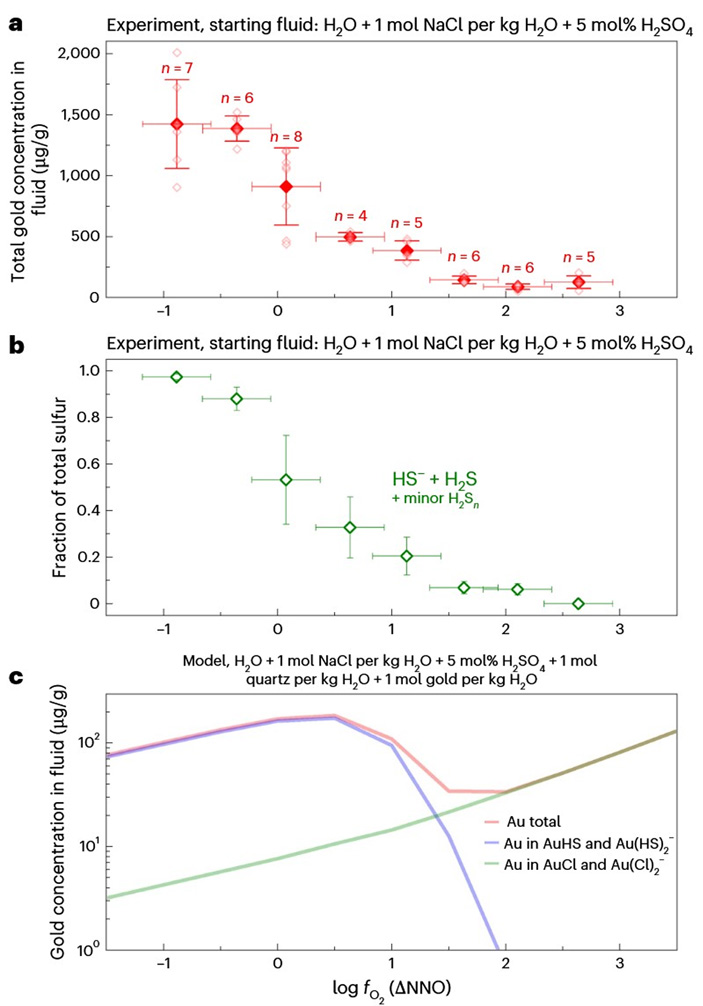
Рис. 6. a — измеренная концентрация золота в различных включениях (по горизонтальной оси — фугитивность кислорода относительно значения буфера Ni-NiO при 2000 бар и 875°C, по вертикальной оси — концентрация золота в мкг/г); b — количество серы, присутствующей в форме HS− и H2S, с небольшой примесью H2Sn (по вертикальной оси — доля от общего количества ионов и соединений серы); c — модельная оценка преобладающих комплексов в серно-хлоридном флюиде при различных значениях фугитивности кислорода (по вертикальной оси — концентрация золота во флюиде в мкг/г, шкала логарифмическая). Графики из обсуждаемой статьи
Наибольшая концентрация золота, до 1420±360 мкг/г, была отмечена в наиболее восстановленных образцах (ΔNNO = −0,9, рис. 6, a), что соответствует комплексам Au(HS)− и AuHS. В окисленных флюидах, более характерных для приповерхностных зон, концентрация золота на порядок меньше — 129±52 мкг/г. Повышенная растворимость золота в присутствии гидросульфидных ионов, а также их преобладание над хлоридными (рис. 6, с) хорошо соответствует предыдущими исследованиям и моделям. Обсуждая этот факт, авторы в предпоследнем параграфе статьи особенно отмечают работу группы из Института геологии рудных месторождений, петрографии, минералогии и геохимии Российской академии наук (ИГЕМ РАН) под руководством Бориса Тагирова, давно изучающей растворимость и транспорт металлов в гидротермальных флюидах.
Завершается статья большой и красивой картинкой предполагаемого серного «зоопарка», сопутствующего островодужной вулканической системе с известково-щелочными магмами (рис. 7). В вулканических газах преобладают H2S и SO2, что хорошо соответствует полевым измерениям (P. Wallace, M. Edmonds, 2011. The Sulfur Budget in Magmas: Evidence from Melt Inclusions, Submarine Glasses, and Volcanic Gas Emissions). В гидротермальных системах, в зависимости от фугитивности кислорода, доминируют HS−, H2S или SO2, а в магматических расплавах — S2− и SO42. На рис. 7 также присутствуют эпитермальные и медно-порфировые месторождения (porphyry copper deposit), которые образуются из вещества, переносимого именно обсуждаемыми в статье флюидами. Отмечу, что несмотря на упоминание месторождений, авторы не приводят конкретных примеров, для которых их результаты могли быть актуальны, или результатов геологического моделирования, ограничиваясь исключительно оценками верхнего предела растворимости золота в изучаемых растворах. То есть, несмотря на геологический контекст этого исследования, оно все же чисто геохимическое.
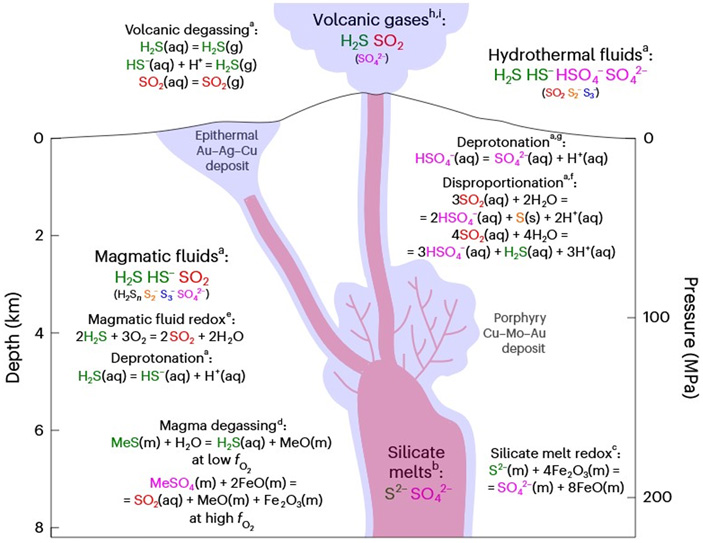
Рис. 7. Островодужная вулканическая система с преобладающими ионами и соединениями серы и важнейшие химические реакции с ее участием. По вертикальной оси: слева — глубина (Depth) в километрах, справа — давление (Pressure) в MPa. Silicate melts — магматические силикатные расплавы, silicate melt redox — окислительно-восстановительное равновесие в силикатных расплавах, Magma degassing — дегазация магмы, Deprotonation — реакция депротонирования, Magmatic fluid redox — окислительно-восстановительное равновесие в гидротермальной системе, Magmatic fluids — магматические флюиды (высокотемпературные гидротермальные растворы), Epitermal Au-Ag-Cu deposit — эпитермальное Au-Ag-Cu месторождение, Volcanic degassing — вулканическая дегазация, Volcanic gases — вулканические газы, Hydrothermal fluids — гидротермальные флюиды (в российской терминологии — средне- и низкотемпературные гидротермальные растворы), Disproportionation — реакция диспропорционирования, Porphyry Cu-Mo-Au deposit — медно-порфировое месторождение. Надстрочные буквы соответствуют литературным источникам, использовавшимся при создании картинки (а — экспериментальные данные авторов). Изображение из обсуждаемой статьи
В тексте обсуждаемой статьи есть достаточно жесткая критика конкурирующей группы Глеба Покровского (Gleb S. Pokrovski) из Университета Тулузы, которая отстаивает важную роль иона S3−, тем самым поддерживая и продолжая давно идущую дискуссию в добрых традициях Nature. Здесь нужно заметить, что в работах группы Покровского используются эксперименты in situ с использованием источников синхротронного излучения, то есть растворы анализируются прямо во время эксперимента и с использованием более чувствительного метода рентгеновской абсорбционной спектроскопии (X-ray absorption spectroscopy). Тонкий контроль за окислительно-восстановительной обстановкой при этом отсутствует, однако технологически его скорее всего возможно добавить в будущем.
Ex situ методы, такие как метод синтетических флюидных включений, часто являются единственным доступным способом изучения растворов при высоких давлениях и температурах, однако, в сравнении с in situ, многое может пойти не так, начиная с потенциальных термических градиентов в капсуле, перекристаллизации включений и потери водорода, если с момента синтеза прошло слишком много времени. Авторы очень компетентно подошли к дизайну эксперимента, однако данные этой статьи вряд ли станут окончательным консенсусом. Скорее, они могут спровоцировать новый виток усовершенствования автоклавов, установленных на таких европейских синхротронах как ESRF (Франция) и DESY (Германия). Этому может воспрепятствовать ограниченная применимость MHC-автоклавов — их используют только до давления 2000 бар и температуры 1100°C. Однако мне кажется, что в ближайшие годы мы совершенно точно увидим дальнейшее развитие метода и новые статьи, проливающие свет на загадочную высокотемпературную химию металлов в гидротермальных растворах.
Источник: Stefan Farsang, Zoltán Zajacz. Sulfur species and gold transport in arc magmatic fluids // Nature Geoscience. 2024. DOI: 10.1038/s41561-024-01601-3.
Кирилл Власов
роль S2− и S3− в гидротермальных растворах была в прошлом переоценена из-за некорректной интерпретации спектров, в которых высокая интенсивность возникала не из-за повышенных концентраций, а благодаря эффекту резонанса.Это же радикалы - молекулы содержащие неспаренный электрон, при этом нет стерических препятствий для димеризации этих радикалов. Как такие радикалы могу иметь высокую концентрацию, чтобы играть какую-то роль в растворимости золота?
По-моему геологи все перепутали - молотки им в руки!
Может они думали, что S2− это аналог супероксид иона, S3− аналог озонид иона? Интенсивный синий цвет лазурита (ультрамарина) обусловлен присутствием анион-радикала трисульфура ( S3−), Присутствие дисульфидного ( S2−) и тетрасульфидного ( S4−) радикалов могут смещать цвет в сторону желтого или красного соответственно.
Но что-то я таких минералов рядом с золотыми месторождениями не видал!
-
-
А в чем проблема? Двухзарядные анионы вполне себе существуют, а если заряд будет находится на разных концах молекулы S6, то электростатическое отталкивание будет компенсировано энергией образования новой связи, тем более в растворителе с диэлектрической проницаемостью ~81.
В серных батарейках идет этот процесс
https://advanced.onlinelibrary.wiley.com/doi/full/10.1002/adma.202306239
и с анализом катионов они без лазера справляются
Другой вопрос что при повышенной температуре идут химические реакции увеличивающие энтропию, т.е. приводящие к распаду сложных молекул на простые...
-
а в магматических расплавах — S2− и SO42.Ещё один минусик оторвалси. :)
за счет минимизации термального бэкграундаРезануло. И не совсем понятно, что за фоновый процесс минимизируется по итогу?..
По сабжу: если я правильно уловил, осаждение усиливается при подъёме за счёт более окислительных условий. Тупо физически, и с этим ничего не поделать (на этом глобусе)... Означает ли это, что до кислородной катастрофы месторождения золота-серебра-меди-др. не формировались по такому механизму (или из-за него..)? Т.е. другие планетоиды, пока не засранные этими гадкими организмусами, могут не иметь кусковых залежей драг-металлов... :з
Ящитаю это прямой повод/вызов загадить организмусами обозримую голактегу!! Целиком!!! >_<
-
Означает ли это, что до кислородной катастрофы месторождения золота-серебра-меди-др. не формировались по такому механизму (или из-за него..
Причем тут кислородная атмосфера? При диспропорционировании Fe+2 в мантии, металлическое железо тонет в ядре, а в мантии остается окисленная форма Fe+3. так же при любых реакциях разложения с образования водорода, он улетает в космос, а окисленные формы остаются в мантии. -
получать спектры высокого разрешения даже при максимальной температуре (875°C) за счет минимизации термального бэкграунда.
Резануло. И не совсем понятно, что за фоновый процесс минимизируется по итогу?..
Рамановская спектроскопия. Спектр получают из уширения частоты рассеянного лазерного излучения. Тепловое излучение с t = 875°C может помешать регистрации сигнала. Поэтому они уменьшили длину волны лазера — стали работать на более высоких частотах, где тепловое излучение намного слабей.Ящитаю это прямой повод/вызов загадить организмусами обозримую голактегу!! Целиком!!! >_<
Где-то щитал, что бактерии причастны к образованию золотых самородков. Поэтому тут без вариантов: голактегу придется загадить. Да прибудет с нами золото!!!11
-
Дык там бактерии жили и фиксировали углерод из углекислого газа.
https://zolotodb.ru/article/10302
Не бывет!!!
Биогенная теория образования месторождений золота
"Ведущая роль биогенных процессов предполагается и при образовании «эндогенных» месторождений золота: (магматических, метаморфических, гидротермальных и пр.). Все они распространены обычно в ассоциации с углеродистыми породами, что является свидетелем происходивших ранее биогенных процессов, в том числе рудообразующих. Биогенные руды, образованные ранее вблизи дневной поверхности, впоследствии, попадая в зоны ультраметаморфизма, преобразовывались в эндогенные месторождения. Источниками золота при их образовании служили не мантия и глубинные флюиды, а первичные биогенные его концентрации. Исключительно абиогенных золоторудных месторождений в земной коре, по-видимому, быть не может, потому, что золото бывает подвижным только в форме золотоорганических соединений, которые образуются только бактериями."
"С представлением о механическом извлечении золота из разрушающихся пород не увязывается, прежде всего, размер самородков и крупного золота в россыпях. В породах – поставщиках золота – самородков весом в единицы и десятки килограмм не бывает."Гном, 12.12.10 11:40:25
Кстати, теория эта не нова. Я слышал о ней ещё в 80-х, когда учился в институте. ...
Месторождение локализовано в углеродистых сланцах, так что с органикой проблем не могло быть.
Или это как-то применимо на практике? Но я не пойму как…
-
Разумеется, применимо на практике: мы можем ожидать месторождений золота в горных породах, омывавшихся восстановительными серосодержащими флюидами. Например, на Меркурии, по данным «Мессенждера», фугитивность кислорода очень низкая, много серы и найдены места, где летучие флюиды доходили в прошлом до поверхности. А значит, теоретическая наука предсказывает, что в данных местах на Меркурии должны быть богатые месторождения золота. С другой стороны, хотя некоторые астероиды тоже подвергались обработке горячими водными флюидами, в результате чего там образовался найденный в метеоритах серпентинит, но там этот процесс протекал в окислительных условиях, о чём свидетельствует наличие большого количества магнетита. А значит, в этих астероидах месторождений золота не будет.
А благодаря вот этой статье можно таки думать, что никто в ближайшем будущем за "своим" золотом сюда не придет.
А прийдет - так оно теперь наше!
Будем кусаться!))
Последние новости

















Рис. 1. Искусственно синтезированные включения гидротермальных водных растворов в кристалле кварца (SiO2), использованные в обсуждаемом исследовании. NNO± — значения относительно минерального буфера Ni-NiO (см. Mineral redox buffer). Включения захвачены при температуре 875°C и давлении 2000 бар, подробнее про методологию исследования см. в тексте. Фотография из обсуждаемой статьи