Чистим кровь полимерной сеткой
Сверхсшитый полистирол в терапии цитокиновой бури
Вадим Даванков, Мария Цюрупа, Людмила Павлова, Александр Пастухов,
институт элементоорганических соединений
имени А. Н. Несмеянова РАН
«Природа» №4, 2021
Более полувека назад мы синтезировали полимер, свойства которого противоречили общепринятым канонам полимерной химии, — сверхсшитый полистирол. Несмотря на жесткую сшивку каждого звена цепи со звеньями соседних цепей, он оказался достаточно эластичным, поглощал большие количества любой жидкости, при этом заметно увеличиваясь в размерах. Сейчас сверхсшитые полистирольные сорбенты производятся тысячами тонн в год, так как нашли множество областей применения в науке и технике. Удивительным свойством жесткой ажурной сетки полимера оказалась ее полная инертность по отношению к клеткам крови и крупным белковым молекулам. Это позволило создать на базе сверхсшитых полимеров универсальные гемосорбенты, которые уже спасли сотни обреченных пациентов с общим заражением крови (сепсисом). В статье рассказывается об этапах создания этих сорбентов, оказавшихся столь востребованными в эпоху текущей пандемии короновируса.
Идею синтеза сверхсшитых полимерных сеток мы сформулировали еще в конце 60-х годов прошлого века, однако серия сорбентов под общим названием «Стиросорб» стала коммерчески доступной только четверть века спустя. Предложенный нами принцип создания жесткой ажурной пространственной полимерной сетки (на примере сверхсшитого полистирола) казался нарушением канонов полимерной химии.
Длинные макромолекулы полистирола достаточно гибки и, растворяясь в таких органических средах, как толуол или дихлорэтан, принимают конформацию рыхлого клубка. Если между макромолекулами полистирола перекинуть сшивающие мостики, то получается пространственная сетка. Такой материал уже нерастворим, но набухает, увеличивая свой объем, в тех жидкостях, в которых растворяется исходный линейный полистирол. Напротив, в метаноле, гексане или воде, в которых линейный полистирол нерастворим, не набухают и его трехмерные сополимеры. Хорошо известна тенденция к снижению способности набухать при увеличении степени сшивания сополимера. Так, если в сополимере стирола с дивинилбензолом доля дивинилбензола увеличивается до 20%, то материал становится жестким, ненабухающим, практически недеформируемым под нагрузкой. Это классика, азы полимерной химии, приведшие к догме, гласящей, что межмолекулярные сшивки уплотняют полимерный материал. Эта догма подтверждалась и переходом от резины к жесткой гуттаперче при увеличении степени сшивки, и всей практикой создания часто сшитых эпоксидных полимеров.
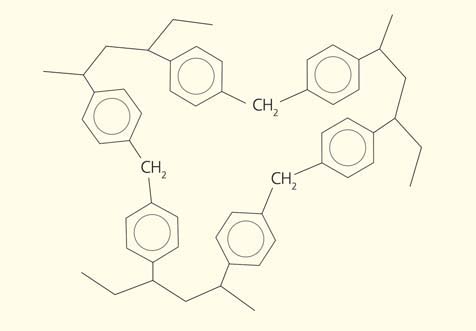
Природа, однако, гораздо богаче самых совершенных теорий, и сшивки, оказывается, могут не уплотнять, а, наоборот, разрыхлять полимерную сетку. Ведь длинные и жесткие спейсеры могут играть роль распорок между элементами сетки. Все зависит от того, каково взаимное расположение цепей и узлов сетки в пространстве (т. е. топология сетки), какова природа сшивок и в каких условиях они возникли между полимерными цепями. Мы создали сверхсшитый полистирол в присутствии хорошего растворителя. В полученной сетке почти каждое мономерное звено полистирола вовлечено в образование одного, а то и двух мостиков к ближайшим соседям (рис. 1), а материал тем не менее имеет низкую плотность, легко деформируется и сильно набухает в любых жидкостях [1]. Это не укладывается в рамки современных теорий, но легко может быть понято, если отказаться от догм и руководствоваться соображениями элементарной логики. Как показывает практика, приверженцы классической полимерной химии не всегда способны совершить этот простой шаг.
Неудивительно, что первоначально принцип создания сверхсшитого полистирола не был принят научной «полимерной» общественностью и в нашей стране, и за рубежом. Однако мы не отчаивались и продолжили доказывать необычные свойства и уникальные сорбционные способности сверхсшитого полистирола как первого представителя принципиально новых полимерных материалов [2, 3].
По истечении срока действия наших патентов в 16 странах мира английская фирма «Purolite» в рамках научно-технического сотрудничества с нашим институтом (ИНЭОС имени А.Н.Несмеянова) уточнила технологию и в короткие сроки организовала промышленное производство нового поколения сорбентов — сверхсшитых полистирольных сорбентов. К сожалению, наши старания активизировать сотрудников химкомбинатов в Черкассах и Олайне окончательно лопнули с развалом Союза и уходом Украины и Прибалтики в свободное пике. Попытка организовать совместное с «Purolite» производство сорбентов в Омске на крупном химкомбинате, создаваемом тогда в нашей стране, в лихие 90-е тоже провалилась. С тех пор уникальные сорбенты в промышленном масштабе производились только в Англии, но потом англичане построили дочерние заводы еще в Румынии и Китае.
Ныне выпускается целая серия сверхсшитых сорбентов, которые основаны либо на микропористых полимерных матрицах, либо на бипористых (рис. 2). Последние содержат кроме очень малых пор еще и крупные транспортные поры, которые пронизывают всю полимерную гранулу. Сорбенты нашли широкое применение в мире во многих промышленных сорбционных технологиях, а также стали незаменимым материалом в аналитической химии для концентрирования чужеродных микропримесей из природных и промышленных воздушных и водных сред.

Рис. 2. Внешний вид гранул сверхсшитых полистирольных сорбентов «MaсroNet» микропористой MN-270 (а), бипористой MN-200 (б) и MN-202 (в) структуры («Purolite», Великобритания)
В 1993 г. в совместной работе с немецким профессором К.К.Унгером [4] по применению микропористого сверхсшитого полистирола в качестве сорбента в аналитической колонке для высокоэффективной жидкостной хроматографии было неожиданно обнаружено, что сорбент поглощает из физиологических жидкостей и при этом разделяет фармацевтические препараты и их метаболиты, но не сорбирует альбумин и другие белки крови. Понятно, что крупные молекулы белков благодаря ситовому эффекту микропористой матрицы не проникают внутрь гранулы. Но почему же белки не сорбируются на внешней поверхности гранул?
В том же 1993 г. было сделано второе важное наблюдение. Один из авторов этих строк (В.А.Даванков) во время трехмесячной работы в качестве приглашенного профессора (англ. visiting professor) в Университете Париж-Север (фр. Université Paris-Nord) под мощным микроскопом увидел, как тромбоциты крови быстро адсорбируются и буквально распластываются на плоской поверхности полистирольной чашки Петри, но не приклеиваются к гранулам нашего сверхсшитого полистирола. Это никак не согласовывалось с известным сродством белков к гидрофобным поверхностям и столь же известной быстрой коагуляцией крови (образованием сгустков) при контакте крови с поверхностью полистирола. Вскоре пришло понимание, что уникальная ажурная молекулярная структура сверхсшитого полистирола не предоставляет ни крупным белковым молекулам, ни клеткам крови (тромбоцитам, лимфоцитам и др.) достаточных участков плоской гидрофобной поверхности для закрепления (вспомним, что липкая лента прочно прилипает к гладким поверхностям, но не клеится к ткани или шершавым поверхностям, например, к наждачной бумаге).
Эти два наблюдения — ситовые свойства в отношении белков крови и тромборезистентность (гемосовместимость) сверхсшитого полистирола послужили отправными точками для создания гемосорбентов на его основе.
Идея была реализована в конце 1990-х годов в созданной в США компании «RenalTech» (от Renal Technologies — почечные технологии). Главный нефролог Нью-Йорка Натан Левин (N.W.Levin), основатель Института исследований почек (Renal Research Institute), четко сформулировал задачу: разработать полимер, который был бы совместим с кровью пациента, не поглощал альбумин и другие важные белки крови, но селективно удалял так называемые малые белковые токсины с молекулярной массой меньше 30 кДа. Задача эта особенно актуальна для США, где насчитывается более 130 тыс. пациентов с «неработающими» почками. Их жизнь поддерживается тремя длительными процедурами гемодиализа в неделю. Гемодиализатор, или искусственная почка, решает главную проблему — за 3–4 ч удаляет из организма излишек воды, который убил бы человека в течение недели. Но через очень тонкие поры мембраны диализатора не удаляются малые белковые токсины, которые со временем приносят больным массу проблем и в итоге сокращают продолжительность его жизни в среднем до пяти лет.
Мы намеревались модифицировать под новую задачу уже выпускаемые в Англии сверхсшитые полистирольные сорбенты. Но организовать сотрудничество между нашим английским партнером «Purolite» и американским партнером «RenalTech» нам не удалось, поэтому пришлось разработать новый тип сверхсшитой сетки — сверхсшитый полидивинилбензол. Вкратце о принципе: сверхсшитая ажурная сетка требует для своего создания присутствия значительных количеств термодинамически хорошего растворителя в качестве среды в процессе введения множества жестких сшивающих мостиков между полимерными цепями. В этих условиях полимерные сегменты, окруженные сольватирующими молекулами растворителя, не сближаются друг с другом и в итоге становятся элементами жесткой ажурной конструкции микропористого материала (рис. 3).
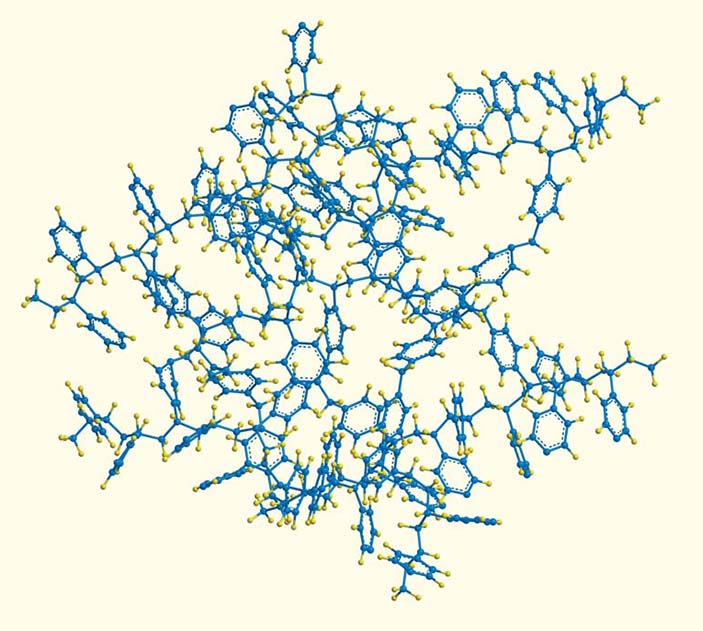
Рис. 3. Схематическое изображение фрагмента трехмерной сверхсшитой полимерной полистирольной матрицы
Но для улавливания малых белковых токсинов в этой сверхсшитой матрице надо было создать еще и более крупные каналы — мезопоры. Придание же мезопористой структуры формирующемуся полимеру, наоборот, возможно только при частичном фазовом распаде полимеризующейся системы, т. е. в присутствии нерастворителя (осадителя полимера) в реакционной среде. Только глубокое понимание механизма образования трехмерных сеток и богатый накопленный опыт позволили нам совместить в едином процессе два этих взаимоисключающих требования.
Мы предложили полимеризовать дивинилбензол в смеси толуола — термодинамически хорошего растворителя — и изооктана — осадителя. «Ноухау» заключается в специфической пропорции двух жидкостей, концентрации дивинилбензола в этой смеси и режиме суспензионной полимеризации.
Итак, нужные ситовые свойства — что извлечь, а что оставить — придаются сорбенту его мезопористой структурой, а гемосовместимость — жесткой ажурной матрицей. Эффективность решения поставленной задачи была продемонстрирована селективностью удаления β2 -микроглобулина из плазмы крови и цельной крови. Этот токсичный белок накапливается в крови почечных больных и откладывается в суставах и сосудах, что и оказывается гибельным для пациентов, находящихся на постоянном гемодиализе. Молекулярная масса этого токсина 12.8 кДа, что вроде бы существенно меньше массы альбумина — 66.5 кДа. Но по размерам токсин всего лишь в два раза меньше молекулы этого основного белка крови. Кроме того, концентрация токсина в 1000 раз меньше концентрации основных белков плазмы. Все же мы смогли сыграть на этом чрезвычайно малом различии в размерах молекул и обеспечить количественную сорбцию токсина при минимальных потерях полезных белков. Гемосовместимость полимерного сорбента обеспечивалась ажурной структурой поверхности гранул сверхсшитого полимера. Мы дополнительно повысили инертность материала прививкой минимального количества гидрофильного N-винилпирролидона на внешней поверхности гранул гидрофобного полидивинилбензола. Полимер успешно прошел в США все клинические испытания и получил название «BetaSorb».
Колонка с «BetaSorb» в США изначально предлагалась для почечных больных и потому использовалась в сочетании с аппаратом искусственной почки, в котором основным звеном, удаляющим воду (и мелкие молекулы типа мочевины), является диализатор. Это картридж, вмещающий пу-чок полых волокон. Через волокна прокачивается кровь пациента, причем стенки волокон являются той самой полупроницаемой мембраной, через которую уходит лишняя вода. Для успешной работы мембран диализатора требуется большая скорость потока крови через картридж — не менее 400 мл/мин. Это — громадная нагрузка для пациента: столько крови можно брать только из артерии (или из вживленного шунта между артерией и веной). Но такая высокая скорость требует и увеличения размера нашей сорбционной колонки (до 300 мл), включенной в цепь последовательно после диализной.
В процессе испытания этой системы оказалось, что наш полимер великолепно удаляет не только β2 -микроглобулин, но и целый набор малых токсичных белковых молекул — цитокинов, а также медиаторов и промоторов воспалительных процессов. Их сейчас уже известно более сотни. Концентрация этих токсинов в крови резко возрастает привоспалительных процессах, особенно при заражении крови — сепсисе. Этот всплеск называют цитокиновым штормом, который приводит к поражению и гибели многих органов пациентов и повышению средней смертности до 60 %. Наш полимер — теперь уже под названием «CytoSorb» — оказался спасительным для больных с сепсисом [5]. Официальные клинические испытания были проведены в Германии на двух группах пациентов по 43 человека каждая. У всех констатировался септический шок с остановкой дыхания. В испытуемой группе в дополнение к стандартному лечению применялась гемосорбция на нашем полимере. За 28 дней (четырехнедельный тест) в этой группе не умер ни один пациент, в контрольной группе, несмотря на проведение стандартной интенсивной терапии, смертность превысила 60 %.
В итоге сверхсшитый полидивинилбензольный «CytoSorb» рекомендован в Европейском сообществе при сепсисе и других острых воспалительных процессах и уже спас много сотен человеческих жизней (рис. 4).
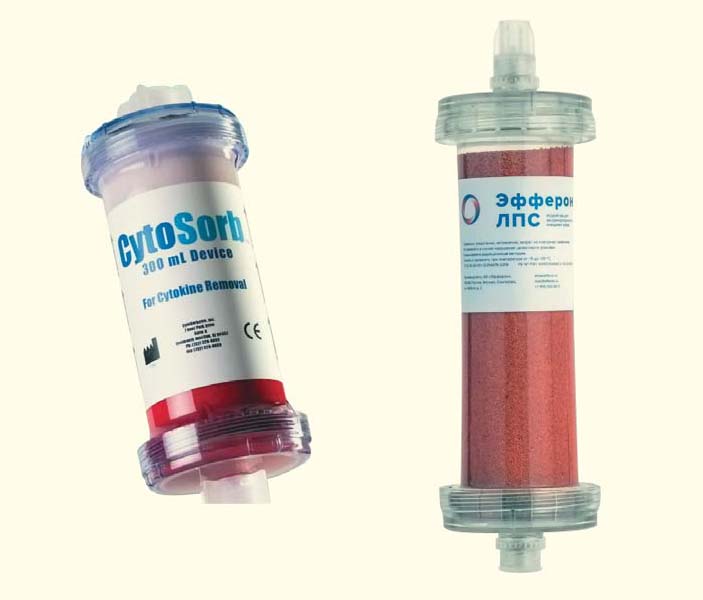
Рис. 4. Используемые в лечении септических пациентов гемосорбенты сверхсшитой структуры: колонка «СytoSorb» (США) со сверхсшитым полидивинилбензолом и колонка «Эфферон-ЛПС» (Россия) со сверхсшитым полистиролом «Стиросорб» и привитыми ЛПС-селективными лигандами
Успехи нашего гемосорбента на западе помогли найти медиков-энтузиастов и в нашей стране. Чтобы не вступать в конфликт с американскими «партнерами» (а там с нашими именами зарегист-рированы 20 патентов [6] на получение и применение полидивинилбензольного гемосорбента), в России мы вернулись к сверхсшитому полистиролу «Стиросорб», на основе которого был создан «Эфферон-ЛПС» (см. рис. 4).
В соответствии с нашей первоначальной идеей сверхсшитый сорбент «Стиросорб» получается дополнительной интенсивной сшивкой гранул на-бухшего в дихлорэтане сополимера стирола с дивинилбензолом, вплоть до введения двух метиленовых «сшивок-распорок» между всеми фенильными кольцами сополимера.
Жесткая ажурная структура конечного материала представляет собой единую систему взаимопроникающих макроциклов самого различного размера. Измеренная стандартным способом сорбции азота удельная поверхность материала колоссальна и приближается к 1000 м2/г, объем пор — 0.5 см3/г. Размер гранул 0.3–1.0 мм. Напомним, для наших целей эта микропористая ажурная сверхсшитая матрица должна быть снабжена еще и мезопорами, которые обеспечивали бы проникновение внутрь гранулы и сорбцию там целевых токсинов размером до 30–50 кДа. Эти каналы матрицы в основном задаются морфологией исходного сополимера стирола с дивинилбензолом. А она в свою очередь — оптимальным подбором содержания дивинилбензола и состава порогена — смеси термодинамически хорошего и плохого растворителей на стадии получения исходного сополимера в виде гранул.
Сделать нужный материал — это даже не полдела. Кто проверит его полезность и продвинет в медицинскую практику?
Сравнительное испытание имеющихся в России гемосорбентов с представленными нами образцами сверхсшитого дивинилбензола и сверхсшитого полистирола «Стиросорб» провел доктор Д.П.Елизаров в Пермской государственной медицинской академии имени академика Е.А.Вагнера (в 2014 г. академии был присвоен статус университета) [7]. Для нашей страны лечение почечных больныхне столь актуально, как в США, у нас парк искусственных почек для поддержания их жизни крайне скуден. А вот острые химические отравления уносят у нас около 50 тыс. жизней ежегодно. Испытания на подопытных крысах и собаках убедительно показали, что «Стиросорб» полностью гемосовместим и великолепно удаляет из крови низко молекулярные отравляющие вещества, четыреххлористый углерод, дихлорэтан, барбитураты и даже полярную фосфорорганику и метанол. Все они легко удаляются микропористой матрицей сорбента, спасая отравившихся животных. По сорбционной активности и особенно по гемосовместимости наш «Стиросорб» намного превосходит все имеющиеся и находящиеся в разработке гемосорбенты. Он также обладает высокой механической прочностью и не крошится, как активированный уголь. Присутствие пылевидных частиц в гемосорбенте недопустимо: они забивают капилляры, прекращая доступ крови к живым тканям и органам.
Несмотря на убедительный успех испытаний на животных, работы в Перми по независящим от нас причинам продолжить не удалось. Но крайне полезное свойство наших сорбентов помогло найти новых партнеров-энтузиастов в Национальном медицинском исследовательском центре онкологии имени Н.Н.Блохина. В этом центре крайне актуальной оказалась борьба с постоперационным сепсисом. Востребованность эффективных и универсальных гемосорбентов в этом случае не вызывала сомнений. Мы предоставили партнерам три образца сверхсшитого полистирола «Стиросорб», различающиеся структурой пор и природой функциональных групп на поверхности.
Многочисленные анализы крови крайне тяжелых онкопациентов убедительно подтвердили высокую клиническую эффективность гемо- и лимфосорбции на сверхсшитом полистироле в допол- нение к комплексной терапии, применяемой в критических случаях. Все образцы сверхсшитых полистирольных сорбентов удаляют из кровотока большинство цитокинов и промоторов воспаления ничуть не хуже, чем сверхсшитый полидивинилбензол «CytoSorb» и любой другой импортный гемосорбент. Более того, было обнаружено, что наши «Стиросорбы» активно ингибируют рост грамположительных бактерий и даже грибов, которые могут появиться в крови при сепсисе [8]. Отлично удаляются из крови и чрезвычайно токсичные липополисахариды (ЛПС) — осколки клеточных оболочек бактерий и собственных убитых клеток организма. Кроме того, значительно снижаются концентрации токсичных малых молекул — мочевины, креатинина и общего билирубина. Наблюдается регуляция гомеостаза на клеточном, тканевом и органном уровнях, что предотвращает развитие органной и полиорганной недостаточности даже при самых неблагоприятных прогнозах. Нормализуются температура, давление, пульс. И при этом нет потери белков плазмы и активации клеток крови [9]. Итак, стало очевидным, что «Стиросорб» обеспечивает комплексную детоксикацию крови.
Однако любые самые полезные устройства и продукты нельзя применить в медицинской практике без прохождения официальных государственных медицинских испытаний. Проверяется не сорбент, а конечное медицинское изделие. Такое изделие — «Колонку гемосорбционную ГемосДС», заполненную «сополимером стирола сверхсшитой структуры по ТУ 6-05-1996-84», удалось создать при активном участии руководителя ООО «Биотех-М» И.Ю.Саркисова. И вот в итоге многолетних усилий в 2013 г. Получена долгожданная путевка в жизнь: «Регистрационное удостоверение на медицинское изделие». Оно теперь рекомендовано к серийному выпуску и использованию в медицинской практике лечебных учреждений РФ.
Результаты длительных государственных медицинских испытаний гласят: «Испытанный сорбент из сополимеров полистирола обладает выраженным положительным воздействием на различные системы гомеостаза, включая липиды крови, цитокиновый и клеточный компоненты и др.». Необходимо обратить внимание на подбор пациентов, на которых проводились официальные испытания. Среди них нет пораженных сепсисом — они изначально считаются обреченными. Испытывают новую технику на давших согласие пациентах с разными не угрожающими жизни заболеваниями — бронхиальной астмой, панкреатитом, атеросклерозом и др. Выраженный положительный эффект наблюдался во всех случаях. Это говорит о чрезвычайно широкой области применения процедуры гемосорбции на нашем сорбенте.
Но в большинстве этих случаев нет необходимости сочетать гемосорбционное устройство с громоздкой и дорогой, к тому же не выпускающейся нашей промышленностью диализной системой — искусственной почкой. А без нее скорость прокачки крови через колонку можно резко уменьшить, как и габариты самой колонки. Сорбционная активность полимера очень высока и потому для детоксикации всего объема крови пациента достаточно применить не более 150 мл сорбента. Такое существенное уменьшение объема (с 300 мл до 150 мл) колонки и, соответственно, (временно) забираемой крови особенно благоприятно при проведении гемосорбции у детей, беременных или истощенных пациентов. Еще важнее то, что малая скорость прокачки жидкости открывает возможность доступа к кровеносной системе не через артерию, а через вену. Теперь любой перистальтический насос с системой микроклапанов и единственной двухканальной иглой позволяют обеспечить двух-трехкратную фильтрацию всего объема крови пациента через сорбционную колонку за пару часов.
Вся аппаратура легко умещается в переносной кейс и может запитываться как от электросети, так и от небольшого аккумулятора. Значит, такую систему можно применять не только в стационаре, но и в любой карете скорой помощи, в домашних и полевых условиях. Она делает возможным оказание экстренной помощи в случае передозировок лекарств и острых и массовых отравлений химическими соединениями, контрафактным алкоголем или наркотиками. В этом отношении новая компактная система гемосорбции представляет несомненный интерес также для служб МЧС, медицины катастроф и военной медицины. Обслуживание системы настолько просто, что его успешно освоили работники ветеринарных служб для спасения домашних животных после укуса энцефалитными клещами и тяжело травмированных скаковых лошадей и породистых собак с развивающимся сепсисом.
И все же частные успехи не заслонили для нас важнейшую цель — создание целевого гемосорбента для успешной борьбы именно с сепсисом. В 2017 г. Всемирная организация здравоохранения объявила сепсис глобальным приоритетом. Действительно, от сепсиса ежегодно погибает 11 млн пациентов, что составляет почти 20% от всех регистрируемых в год смертельных случаев.
В продвижении наших разработок весьма полезным оказался союз с молодыми энтузиастами под руководством И.В.Бессонова, которые создали компанию «Перспективные медицинские технологии». В их активе была разработка лиганда, специфичного к ЛПС. Эти крайне токсичные продукты распада клеточной оболочки патогенных бактерий вызывают гиперактивацию иммунного ответа организма септического больного и выброс в кровоток громадного количества цитокинов, медиаторов и промоторов воспалительных процессов (цитокиновый шторм) и, как следствие, отказ функционирования многих жизненно важных органов больного. Распад одной бактериальной клетки выбрасывает в кровоток порядка миллиона фрагментов ЛПС. Химическая фиксация ЛПС-связывающих специфических лигандов в порах сверхсшитой полистирольной матрицы сорбента резко повысила его способность удалять из крови липополисахариды. При этом сорбент сохраняет свою изначально уникальную сорбционную емкость как по цитокинам — низкомолекулярным токсичным белкам, так и по разнообразным химическим ядам. Таким образом, новая модификация сверхсшитого полистирольного гемосорбента «Эфферон-ЛПС» осуществляет комплексную детоксикацию крови.
Пандемия COVID-19 резко увеличила количество пациентов с тяжелым поражением легких и даже сепсисом, и потому гемосорбент «Эфферон-ЛПС» оказался особенно востребованным. И вот в конце 2020 г. в престижнейшем медицинском журнале появляется статья медиков (Городская клиническая больница No1 имени Н.И.Пирогова и НИИ общей реаниматологии имени В.А.Неговского), в которой подробно изложены результаты лечения девяти тяжелых пациентов с септическим шоком с применением колонки «Эфферон-ЛПС» [10].
Через сорбент прокачивалось от четырех до пяти объемов циркулирующей крови пациентов со скоростью 100–150 мл/мин в течение 4–6 ч. Даже однократная процедура гемоперфузии приводила к значительному снижению содержания в крови как ЛПС, так и основных токсичных цитокинов, что указывает на комплексный, мультимодальный характер лечебного действия сорбента. Выраженный противошоковый эффект наблюдали у семи пациентов, в то время как быстрого эффекта не удалось добиться у двух особенно тяжелых пациентов, вскоре погибших. В итоге реаниматологи подтвердили «перспективность проведения дальнейших клинических исследований колонки «Эфферон-ЛПС», содержащей мультимодальный гемосорбент на основе сверхсшитого стирол-дивинилбензольного сополимера с иммобилизованным ЛПС-селективным лигандом, для экстракорпоральной детоксикации пациентов с септическим шоком» [10].
Известно, что внедрение самых перспективных методов и технологий надолго сдерживается слишком медленным распространением информации в сообществах потенциально заинтересованных специалистов. Об этом ярко свидетельствует вся история сверхсшитых полимерных материалов, которая насчитывает уже более полувека. Поскольку компания «Эфферон» в 2020 г. предоставила отечественным клиникам несколько сотен колонок с нашим сорбентом, стоит надеяться, что за первой публикацией реаниматологов последуют другие. Очень хочется верить, что продвижение в жизнь разработанных нами отечественных сверхсшитых гемосорбентов пойдет ускоренными темпами.
Впрочем, уникальная структура и свойства сверхсшитых полимеров, необязательно полистирольной или полидивинилбензольной природы, открывают широкие возможности для разработки новых сорбентов, например, для борьбы с хроническими заболеваниями почек, печени, сердечно-сосудистой системы и т. п. Высокая активность полимера в сочетании с современной тенденцией к миниатюризации и автоматизации медицинских устройств могут послужить предпосылкой к созданию портативных приспособлений типа носимой буквально в кармане «искусственной почки», запатентованной нами еще в 1996 г. [11].
Не исключено, что в ближайшем будущем молодые энтузиасты откроют новые аспекты применения сверхсшитых полимеров в медицине и не только в ней.
Литература:
1. Даванков В.А., Цюрупа М.П., Пастухов А.В. и др. Сверхсшитый полистирол: Чужой среди своих. Российская наука. Выстоять и возродиться. М., 1997; 182–187. [Davankov V.A., Tsyurupa M.P., Pastukhov A.V. et al. Supercrosslinked polystyrene: an alien its own class. Russian Science: Withstand and Rivive. Moscow, 1997; 182–187. (In Russ.).]
2. Tsyurupa M.P., Davankov V.A. Hypercrosslinked polymers: basic principle of preparing the new class of polymeric materials. Reactive & Functional Polymers. 2002; 53(2–3): 193–203. DOI:10.1016/S1381-5148(02)00173-6.
3. Цюрупа М.П., Блинникова З.К., Павлова Л.А. и др. Сверхсшитому полистиролу полвека: от нетривиальной идеи до промышленной реализации. Лаборатория и производство. 2020; 11(1): 86–96. [Tsyurupa M.P., Blinnikova Z.K., Pavlova L.A. et al. Hypercrosslinked polystyrene: half a century from a non-trivial idea to industrial implementation. Laboratory and Production. 2020; 11(1): 86–96. (In Russ.)] DOI:10.32757/2619-0923.2020.1.11.86.96.
4. Beth M., Unger K.K., Tsyurupa M.P., Davankov V.A. Microporous hypercrosslinked polystyrene as a restricted access packing in sample clean-up for high performance liquid chromatography. Part I: Evaluation of restricted access property. Chromatographia. 1993; 36: 351–355. DOI:10.1007/BF02263890.
5. Winchester J.F., Ronco C., Brady J.A. et al. The next step from high-flux dialysis: application of sorbent technology. Blood Purif. 2002; 20: 81–86. DOI:10.1159/000046989.
6. Brady J.A., Winchester J.F., Davankov V.A., Tsvurupa M.P., Pavlova L.A., Norris F.M., Quartararo P.J., Salsberg J.A. Methods for reducing levels of pro-inflammatory or anti-inflammatory stimulators or mediators in the blood. Patent USA 8,349,550; 2013.
7. Елизаров Д.П., Елькин А.И., Даванков В.А. и др. Изучение сорбционной активности адсорбентов в эксперименте. Токсикологический вестник. 2003; 2: 18–21. [Elizarov D.P., Elkin A.I., Davankov V.A. et al. Study of the sorption activity of adsorbents in the experiment. Toksikologicheskii Vestnik. 2003; 2: 18–21. (In Russ.)]
8. Anisimova N.Yu., Dolzhikova Yu.I., Davankov V.A. et al. Prospects for the application of biporous sorbents based on hypercrosslinked styrene polymers for the prevention and treatment of systemic purulent-septic complications. Nanotechnol. Russia. 2012; 7(5–6): 318–326. DOI:10.1134/S1995078012030020.
9. Davankov V.A., Tsyurupa M.P., Pavlova L.A. Chapter 4: Detoxification of Blood and Plasma by Means of Hypercrosslinked Polymeric Hemosorbents. Immunopathogenesis of Sepsis and Use of the Hemosorption for Treatment of Cancer Patients with Sepsis. N.Yu.Anisimova (ed.). N.Y. (USA), 2014; 57–113.
10. Магомедов М.А., Ким Т.Г., Масолитин С.В. et al. Использование сорбента на основе сверхсшитого стирол-дивинилбензольного сополимера с иммобилизованным ЛПС-селективным лигандом при гемоперфузии для лечения пациентов с септическим шоком. Общая реаниматология. 2020; 16(6): 31–53. [Magomedov M.A., Kim T.G., Masolitin S.V. et al. Use of sorbent based on hypercrosslinked styrene-divinylbenzene copolymer with immobilized LPS-selective ligand in hemoperfusion for treatment of patients with septic shock. General Reanimatology. 2020; 16(6): 31–53. (In Russ.).] DOI:10.15360/1813-9779-2020-6-31-53.
11. Даванков В.А. Искусственная почка. Патент РФ 2 068 707 (1996). [Davankov V.A. Artificial Kidney. Russ. Pat. 2 068 707 (1996).]































Рис. 1. Структура минимального цикла трехмерной сетки, образованная тремя –СН2-мостиками между звеньями трех полистирольных цепей