Спасительная свинья
Елена Клещенко
«Химия и жизнь» №2, 2022
Человеку впервые трансплантировали сердце генно-модифицированной свиньи. Прошел месяц, и этот человек, умиравший от сердечной недостаточности, все еще жив. Кроме того, провели эксперимент по пересадке почек человеку с умершим мозгом от такой же свиньи. Значит ли это, что трансплантация органов, взятых у животных, стала реальностью?
— Он хотел жить. Знал, что помрет, — и все равно хотел. Ему надо было каких-то там вшивых пятьдесят тысяч за комплекс «сердце — легкие» от трансгенной свиньи и за лечение. Он копил — по пять, по двадцать, по полсотни бассов, сколько получал на сталкинге, а зарабатывать сил уже не было.
Александр и Людмила Белаш.
Кибер-вождь (2002)
В не особенно светлом, но высокотехнологичном будущем фантастического романа супругов Белаш (кстати, оба автора — врачи) единственное препятствие для трансплантации жизненно важных органов от генно-модифицированного животного — деньги. Их у несчастного героя нет, но это другой вопрос, а все технические трудности, по-видимому, разрешены века назад. То есть сейчас, при нашей жизни. Посмотрим, как это происходит.
Что случилось
Незадолго до нового 2022 года Управление по контролю качества продуктов и медикаментов США (FDA) приняло беспрецедентное решение: разрешило пересадить человеку сердце генно-модифицированной свиньи, созданной в компания «Revivicor». Медицинское вмешательство, не прошедшее клинические исследования, в США возможно как «терапия сострадания», если это единственный вариант для пациента, которому угрожает смерть.

Дэвид Беннет с семьей
Пациент — Дэвид Беннет, страдающий неизлечимой болезнью сердца, — был госпитализирован с опасной для жизни аритмией и более шести недель подключен к аппарату искусственного кровообращения. Сердце свиньи ему трансплантировали 7 января сотрудники Школы медицины Университета Мэриленда в Медицинском центре Университета под руководством кардиоторакального хирурга Бартли Гриффита. На момент подготовки статьи пациент жив, в пресс-релизе от 28 января сообщается, что ему понемногу становится лучше, он делает гимнастику и спрашивает, когда можно будет поехать домой.
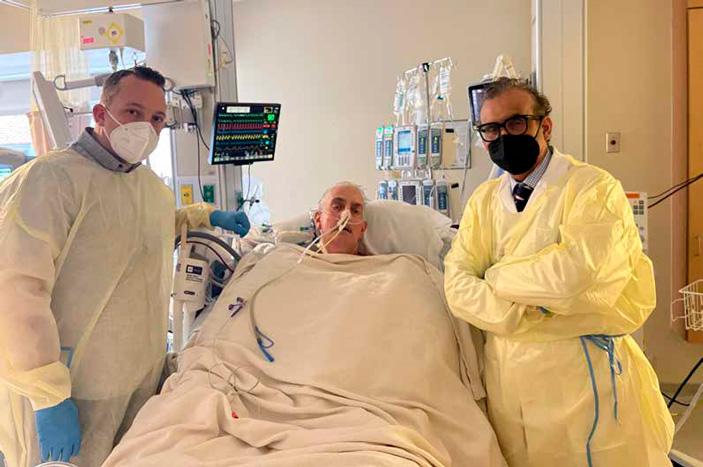
Дэвид Беннет с сыном и доктор Мухаммад Мохиуддин, профессор хирургии и научный директор программы по ксенотрансплантации школы Медицины Университета Мэриленда
Пресс-релиз о пересадке сердца вышел 10 января, а 20 января появилось еще одно сенсационное сообщение: в октябре ученые из Университета штата Алабама в Бирмингеме провели эксперимент по трансплантации генетически модифицированных свиных почек человеку. Свинью предоставила та же компания «Revivicor». В этом случае речь идет именно об эксперименте, а не о спасении жизни, поскольку к моменту пересадки мозг человека умер. Реципиент, Джеймс Парсонс, был согласен, чтобы его органы использовали для пересадки или экспериментов. Когда он погиб, семья разрешила держать тело на аппарате искусственного жизнеобеспечения. Эксперимент продолжался трое суток, затем пересаженные почки и организм человека всесторонне исследовали. Результаты опубликованы в «American Journal of Transplantation».
Аналогичный эксперимент с пересадкой почек свиньи от «Revivicor» в человеческое тело с умершим мозгом прошел в сентябре в Медицинском центре Лангон Хелс Университета Нью-Йорка. Но этот эксперимент был подготовительным и выглядел менее элегантно: чтобы решить проблемы с иммунным ответом, вместе с почками пересаживали тимус (вилочковую железу) свиньи.
Реципиенты
Дэвида Беннета, 57-летнего разнорабочего из Мэриленда, отказывались ставить в лист ожидания на трансплантацию сердца — с его сердечной недостаточностью и аритмией это выглядело бесперспективным, как и имплантация искусственного механического насоса.
Ему рассказали о том, что процедура пересадки свиного сердца — экспериментальная, риски ее невозможно оценить. «У меня выбор — умереть либо сделать эту трансплантацию. Я хочу жить. Я знаю, что это выстрел вслепую, но это мой последний шанс», — сказал Дэвид Беннет за день до операции. Говорил он также, что ему надоело лежать на больничной койке, очень хочется встать и, в общем, ничего хуже смерти с ним не случится.
Образ отважного добровольца подпортила пресса: за этот месяц выяснилось, что Дэвид Беннет в 1988 году был осужден за нанесение ножевых ранений некоему Эдварду Шумейкеру, у которого сидела на коленях жена Беннета. Шумейкеру было 22 года, Беннету, очевидно, примерно столько же. Будущий реципиент свиного сердца «в приступе ревнивой ярости» несколько раз ударил Шумейкера ножом в спину, в результате тот остался парализованным до конца жизни. Беннет был приговорен к десяти годам тюремного заключения. Об этом рассказала журналистам сестра жертвы Лесли Шумейкер Дауни; сам Эдвард умер в 2007 году после инсульта.
Родственники жертвы заявляли, что считают Беннета недостойным операции и лучше бы ГМ-сердце досталось кому-нибудь другому. Команда специалистов по трансплантации на это ответила, что криминальное прошлое человека не может быть основанием для отказа в медицинской помощи. И если операция в итоге будет признана успешной — опыт Беннета поможет спасти людей, и его теперешние страдания (а жизнь после такой операции нелегка, даже когда сердце человеческое) хотя бы отчасти искупят зло, которое он причинил.
Команда из Университета Алабамы, пересадившая почки, подчеркивает, что эксперимент не состоялся бы без благородного поступка Джеймса Парсонса. Человеку, которому посмертно пересадили почки свиньи, тоже было 57 лет, по словам родных и близких, он был лихим и авантюрным, но все его любили. Парсонс увлекался гонками по бездорожью на мотоцикле и был зарегистрированным донором органов — очевидно, адекватно оценивал свой уровень риска. В конце сентября он попал в аварию, получил множественные травмы и скончался.
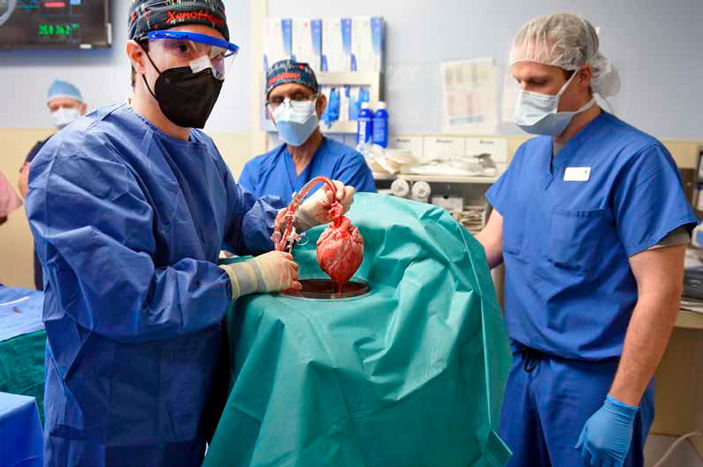
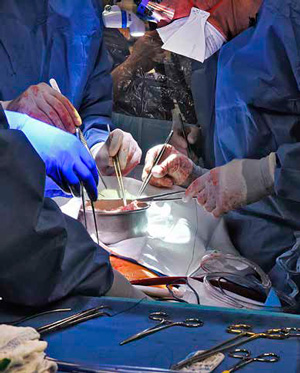
Сердце готово к пересадке
Органы его признали непригодными для пересадки, но 30 сентября 2021 года его семья дала разрешение на эксперимент с почками свиньи. Авторы исследования предлагают назвать этот доклинический протокол испытания ксенотрансплантата «моделью Парсонса».
Были серьезные сомнения, сможет ли почка свиньи полноценно работать в организме человека. У свиней среднее артериальное давление ниже, чем у взрослых людей, а значит, сосуды в почках могли оказаться неприспособленными для жизнедеятельности в человеческом теле. Однако почки оставались жизнеспособными на протяжении 77 часов, продуцировали мочу (одна лучше, другая хуже). Признаков отторжения не наблюдалось, серьезных эпизодов кровотечения не было, но биопсия выявила тромботическую микроангиопатию, причины которой нужно будет изучить. Основные препятствия для трансплантации почки человеку от свиньи преодолены, считают авторы исследования.
История вопроса
Ксенотрансплантация — пересадка органов, тканей или клеток от доноров другого биологического вида — многовековая мечта человечества. Собственно, и трансплантация от человека к человеку стала возможной лишь после того, как иммунология объяснила причины многочисленных неудач и появилось понятие об иммуносовместимости донора и реципиента. Пересадка органа от животного может спасти жизни тысяч людей, ожидающих очереди на донорский орган. (Не говоря о моральной стороне вопроса: жутко ждать чьей-то смерти, чтобы жить самому.) Но в случае трансплантации человек — человек поиск совместимого донора стал задачей, в принципе решаемой: порядок действий понятен, инструменты есть. А что касается органов животных, к решению подступились только сейчас.
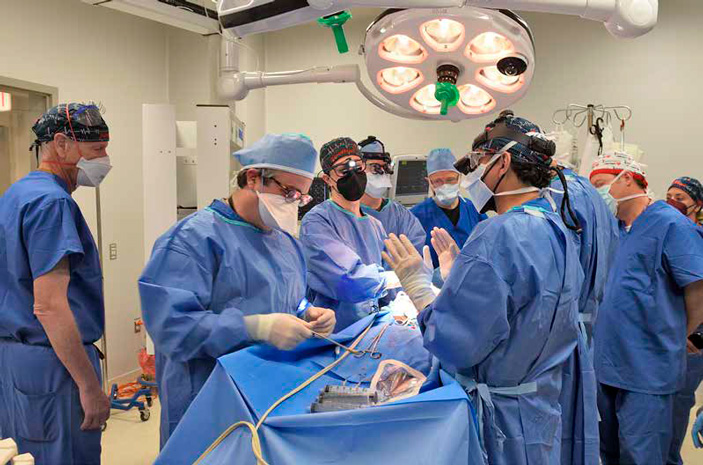
Во время операции
Существует множество историй о попытках ксенотрансплантации в доиммунологическую эпоху. Из статьи в статью кочует рассказ о голландском хирурге Йобе ван Меекрене, который якобы еще в 1682 году пересадил русскому солдату фрагмент собачьей кости, чтобы закрыть повреждение в черепе, но потом был вынужден удалить «трансплантат», потому что солдата, опоганенного собакой, не допускали к причастию. Другие уточняют, что ван Меекрен не сам делал пересадку, а пересказал в своей книге отчет миссионера Йоханнеса Краанвинкеля об операции, выполненной в России, и книга эта на голландском вышла существенно раньше — в 1668 году.
Так или иначе, достоверных сообщений об успешных ксенотрансплантациях нет. Даже в ХХ веке такие попытки кончались плохо. В 1960-е годы Кейт Римтсма из Тулейнского университета в Новом Орлеане пересадил почки шимпанзе трем пациентам — почки отказали во всех случаях, правда, одна пациентка прожила девять месяцев, вернулась к работе школьной учительницей, но потом внезапно потеряла сознание и умерла. При вскрытии почки шимпанзе выглядели нормально, однако симптомы указывали на острое нарушение баланса электролитов. Известно, что почки высших приматов, пересаженные человеку, активно выделяют мочу сразу после операции, в данном случае резкая потеря жидкости, вызвавшая дисбаланс, могла начаться позже. Кейт Римтсма позднее участвовал в создании первого искусственного сердца, но это уже другая история.
Сердце шимпанзе человеку впервые пересадил Джеймс Харди, впечатленный успехами Римтсма. Ксенотрансплантации выполнял и знаменитый южноафриканский хирург Кристиан Барнард, первый, у кого пациенты с пересаженным человеческим сердцем жили десятилетиями. Кстати, Барнард называл своим учителем советского хирурга Владимира Демихова (см. «Химию и жизнь», 2010, 11).
От попыток пересадить человеку сердце животного надолго отказались после случая Стефани Фэй Боклер Трафаган, более известной в истории медицины как «беби Фэй». Девочке, родившейся со смертельным заболеванием сердца — синдромом гипоплазии левых отделов, — в калифорнийском Университете Лома Линда трансплантировали сердце бабуина. Предполагалось потом заменить это сердце на человеческое, но Фэй не смогла его дождаться: через 21 день она умерла от сердечной недостаточности из-за отторжения трансплантата. Бабуин-донор не совпадал даже по группе крови: у Фэй была 0, а у обезьяны АВ, но группа 0 у бабуинов крайне редкая. (Заметим, что Дэвид Беннет уже прожил дольше, чем малышка Фэй.) Случай вызвал бурные дебаты, и было решено, что ксенотрансплантации сердца следует делать только в рамках клинических испытаний . Леонард Ли Бейли, хирург, проводивший операцию, через год выполнил успешную трансплантацию человеческого сердца младенцу.
Неудачными были попытки пересадки кожи и других тканей свиней. А как же клапаны сердца? — спросят многие. Соединительные ткани животных — сухожилия, хрящи, сердечные клапаны — могут служить материалом для трансплантации, но их очищают от клеток (то есть от антигенов, которые могут вызвать иммунную реакцию). Предпринимались попытки реконструкции миокарда человека с помощью внеклеточного матрикса миокарда свиньи — но не целого сердца.
От клонированной овцы до гипоаллергенной свиньи
Если человеческий организм не хочет принимать ткань животного, почему бы не изменить животное? В XXI веке это вполне реальный проект. Генетически модифицированных свиней для трансплантации создали в компании «Revivicor Inc.» из Блэксбурга, штат Виргиния. «Revivicor» — дочерняя организация шотландской биотехнологической компании «PPL Therapeutics», той самой, которая участвовала в создании овечки Долли, первого в мире млекопитающего, клонированного из неполовой клетки взрослого животного.
Год назад «Revivicor» уже попадала в новости, когда ее генно-модифицированных свиней GalSafe одобрило FDA в качестве источника гипоаллергенного мяса и биомедицинских продуктов. Мясо таких свиней не содержит углевода альфа-гал (дисахарида из двух молекул галактозы), который присутствует в мембранах клеток большинства млекопитающих, кроме человека, человекообразных обезьян и приматов Старого Света.
Альфа-гал может вызывать у некоторых людей аллергические реакции (см. «Химию и жизнь», 2020, 12). Эта аллергия возникает после укуса клеща, который перед этим сосал кровь животного. В слюне клеща содержится альфа-гал, когда он попадает в кровь человека, иммунная система запоминает этот углевод как чужеродный, и при последующих контактах с ним развивается характерная реакция — анафилаксия, отеки, крапивница. Необычно, что происходит это через часы после того, как человек съел говядину, баранину или свинину, возможно, потому что аллергенный углевод замаскирован липидами мембраны и медленно поступает в кровоток.
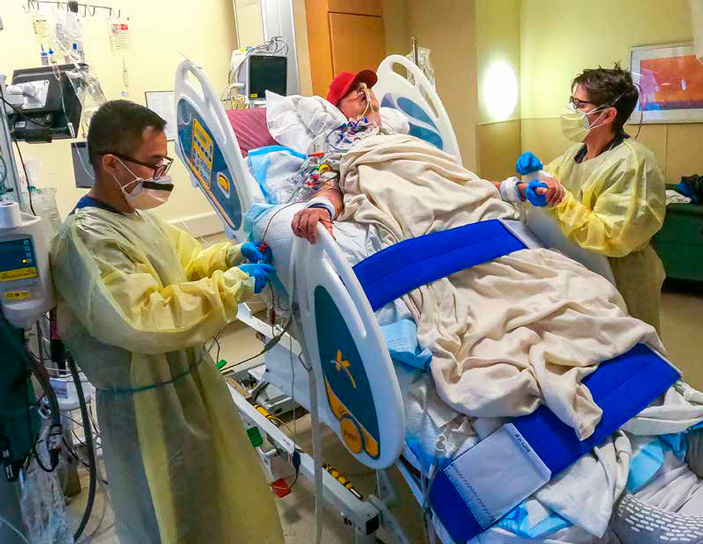
Начало реабилитации на кровати-вертикализаторе
Компания «Revivicor» взялась за эту разработку, конечно, не ради того, чтобы укушенные клещами могли поесть мяса. Людям с аллергией на альфа-гал нельзя назначать лекарства на основе белков, которые производятся в клетках животных. Более того, иммунный ответ на альфа-гал — одна из основных причин отторжения трансплантатов, и это уже касается не только аллергиков.
Идея создать не просто клонированных, а генно-модифицированных животных в PPL возникла практически сразу. Собственно, и Долли появилась на свет из клетки молочной железы (и названа была в честь певицы Долли Партон, знаменитой именно этими частями тела), потому что эти клетки у ученых уже были — с ними экспериментировали, чтобы понять, какая модификация увеличит выработку белков в составе овечьего молока, нужных для медицинских целей.
Вслед за Долли, другими овечками и коровой на свет появились клонированные генно-модифицированные поросята («Nature Biotechnology», 2002, 20, 251–255). И здесь уже начинается история новой сенсации, потому что у этих поросят был поврежден ген фермента GGTA1, синтезирующего альфа-гал. (У нас и обезьян тоже нет именно этого гена, потому и нет этого углевода.) Технологии CRISPR-Cas тогда, естественно, не существовало, ген был инактивирован методом гомологичной рекомбинации.
Работу выполнили Дэвид Айарес и его коллеги из «PPL Therapeutics». Вскоре после этого PPL выделила «Revivicor» в самостоятельную компанию, сейчас Дэвид Айарес занимает в ней пост директора по науке и дает комментарии по поводу трансплантации сердца. В свою очередь, «Revivicor» в 2012 году была приобретена компанией «United Therapeutics», которая запустила программу по разработке ксенотрансплантации почек, а затем сердца и легких. Аллотрансплантацией (от человека к человеку) она тоже занимается. Среди ее проектов есть такие необыкновенные, как «We Fly For Life» — доставка органов для трансплантации по воздуху, на дроне. Звучит эксцентрично, но, если вспомнить, сколько людей умирает в ожидании органа из-за пробок на улицах большого города, — идея здравая.
Именно «United Therapeutics» в 2016 году предоставила Университету штата Алабама в Бирмингеме пятилетний грант для запуска инновационной программы ксенотрансплантации почек. Компания также поддерживала эксперименты по трансплантации сердца генно-модифицированной свиньи бабуинам. Еще в 2016 году удалось показать, что свиные сердца, подсаженные павиану в брюшную полость (не вместо его собственного сердца, а в добавление к нему, просто чтобы проверить жизнеспособность органа), могут оставаться живыми до трех лет.
После того как FDA выдало разрешение на свинью без альфа-гал, Айарес сказал в комментарии журналу «Nature», что они планируют начать клинические испытания трансплантации свиных органов человеку в ближайшие год-два. Варианта с «терапией сострадания», конечно, тогда никто предвидеть не мог.
Как гуманизировать свинью
Первую попытку — нью-йоркский эксперимент с пересадкой почек и тимуса — выполнили на свинье GalSafe. Но почки для второй попытки и, конечно, сердце получили от другой линии свиней, у которых изменены не один, а десять генов. Во-первых, помимо GGTA1, отключены гены @4GalNT2 и CMAH — еще два фермента, которые синтезируют на поверхности клеток иммуногенные углеводы, способные вызвать отторжение трансплантата. Интересно, что эти свиньи — «универсальные доноры»: у них на эритроцитах нет антигенов групп крови. Во-вторых, отключен ген гормона роста, чтобы предотвратить чрезмерное разрастание тканей сердца. (Свиное сердце к гормонам приматов вполне чувствительно.) В-третьих, в геном свиньи добавили шесть человеческих генов. Два из них кодируют ингибиторы системы комплемента, то есть снижают агрессивность человеческой иммунной системы по отношению к пересаженному органу. Продукты еще двух генов регулируют свертываемость крови и должны предотвращать образование микроскопических сгустков крови в пересаженном органе. (Судя по результату с почками, предотвратили не совсем, но эксперименты на обезьянах показывают, что без этой модификации все еще хуже.) Наконец, еще два гена нужны для снижения воспаления и подавления апоптоза в трансплантате.
Тем не менее пациентам понадобятся препараты, подавляющие иммунный ответ. Дэвид Беннетт, как сообщается в пресс-релизе Университета Мэриленда, наряду с обычными иммуносупрессорными препаратами получает новый экспериментальный препарат производства «Kiniksa Pharmaceuticals».
Кроме того, перед экспериментом по пересадке почек реципиент с мертвым мозгом и животное-донор прошли тест на совместимость (чтобы проверить, нет ли у реципиента антител, которые реагируют с антигенами свиньи-донора, сыворотку крови человека смешивают с лимфоцитами донора). Вероятно, подобные тесты делали и перед пересадкой сердца.
Генно-модифицированных животных для трансплантации получают и другие компании, и научные центры, и они используют сходные идеи — в частности, нокаутируют у свиньи те же три гена, отвечающие за иммуногенность. В начале 2000-х годов компания «Xeno Therapeutics» организовала клинические испытания трансплантации кожи от миниатюрной свиньи с дефицитом альфа-гал, которую сделала компания «Immerge Bio Therapeutics». Это тоже была «трансплантация ожидания» — чтобы помочь человеку с обширными ожогами дождаться человеческой кожи.
Есть и еще одна проблема. В геноме свиньи содержатся эндогенные ретровирусы — встроенные вирусные геномы, которые теоретически могут оттуда «выскочить» и начать портить геном человека. Очисткой свиного генома от ретровирусов занимается команда знаменитого гарвардского генетика Джорджа Черча. Черч и его ученица Лухань Янг основали две компании, которые занимаются ксенотрансплантацией, «Qihan Biotech» и «eGenesis». В 2019 году они представили научной общественности своих свиней — не только гуманизированных (три нокаута свиных генов, девять добавленных человеческих), но и свободных от свиных ретровирусов; все они были инактивированы с помощью CRISPR-Cas. Но конкуренты из «Revivicor» успели раньше.
Не все исследователи согласны, что эндогенные ретровирусы вообще влияют на безопасность трансплантации: по их мнению, лучше бы уделить больше внимания обыкновенным свиным вирусам и бактериям, потенциально опасным для человека. Об этом «Revivicor» не забывает: свиньи-доноры живут в специальном питомнике, их ежемесячно проверяют на инфекции, от гриппа до цитомегаловируса. При пересадке почек «перескоков» свиного ретровируса в ткани донора зафиксировано не было, как и других вирусов; в крови реципиента не обнаружено свиных клеток.
Делать окончательные выводы, по-видимому, еще рано. Надо посмотреть, как будет выздоравливать человек со свиным сердцем, как пройдут клинические испытания по трансплантации почек живым людям. В течение ближайшего года станет понятнее, разрешится ли навсегда проклятая проблема дефицита донорских органов. Или же, как сказал один язвительный комментатор, «ксенотрансплантация — дело ближайшего будущего и всегда будет делом ближайшего будущего»?















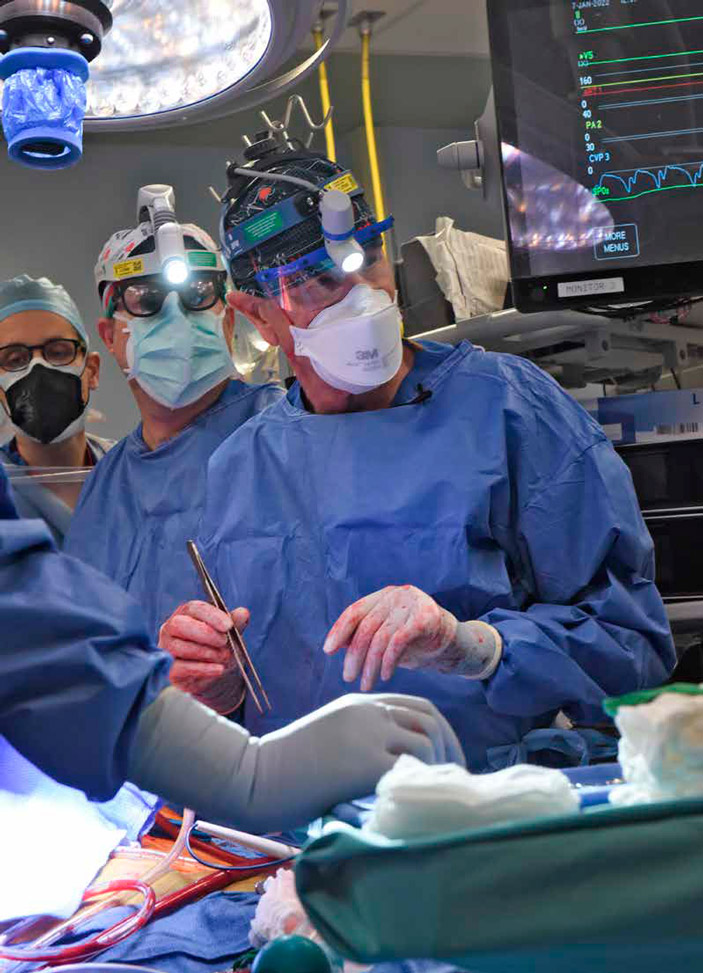
Бартли Гриффит во время операции